题目内容
4.已知A、B、C、D、E五种短周期主族元素,原子序数依次增大,其中A与C、B与D分别同主族,且B原子的最外层电子数等于A与C原子序数之和的一半.下列叙述正确的是( )| A. | 原子半径:A<B<C<D<E | |
| B. | D、E的气态氢化物的热稳定性:D>E | |
| C. | C可与另外四种元素能够分别形成单原子核阴离子的离子化合物 | |
| D. | A与B、C与B均能形成X2Y2型化合物,且其中所含有的化学键类型相同 |
分析 已知A、B、C、D、E五种短周期主族元素,原子序数依次增大,其中A与C、B与D分别同主族,且B原子的最外层电子数等于A与C原子序数之和的一半,若A、C位于ⅡA族,则A与C原子序数之和的一半为8,不满足B为主族元素,则A、C只能位于ⅠA族,A为H、C为Na,则B原子的最外层电子数为:$\frac{1+11}{2}$=6,则B为O、D为S;根据原子序数大小可知E为Cl元素,据此进行解答.
解答 解:A.电子层越多,原子半径越大,电子层相同时核电荷数越大,原子半径越小,则原子半径大小为:A<B<E<D<C,故A错误;
B.非金属性越强,对应氢化物稳定性越强,非金属性D(S)<E(Cl),则气态氢化物的热稳定性:D<E,故B错误;
C.C为Na元素,Na能够与H、O、S、Cl元素形成单原子核阴离子的离子化合物,故C正确;
D.A与B形成X2Y2型化合物为H2O2,C与B能形成Na2O2,但双氧水为共价化合物,过氧化钠为离子化合物,形成化合物中含有化学键类型不同,故D错误;
故选C.
点评 本题考查位置、结构与性质关系的应用,题目难度中等,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题有利于提高学生的逻辑推理能力.

练习册系列答案
相关题目
12.下列元素的基态原子中最难失去电子的是( )
| A. | F | B. | O | C. | Ne | D. | He |
19.在无色透明的溶液中能大量共存的一组离子是( )
| A. | Cu2+、K+、NO${\;}_{3}^{-}$、Cl- | B. | Na+、K+、OH-、Cl- | ||
| C. | Mg2+、Na+、OH-、SO${\;}_{4}^{2-}$ | D. | Ba2+、H+、CO${\;}_{3}^{2-}$、OH- |
9.黄酒又叫老酒,越陈越香,越陈越好,因为黄酒中醇与有机酸反应.该过程中发生的反应为( )
| A. | 取代反应 | B. | 氧化反应 | C. | 加成反应 | D. | 加聚反应 |
16.下列俗名和化学式不吻合的是( )
| A. | 明矾 KAl(SO4)2•12H2O | B. | 重晶石 BaSO4 | ||
| C. | 熟石膏 2CaSO4•H2O | D. | 绿矾 CuSO4•5H2O |
13.铁镍蓄电池又称爱迪生电池.放电时的总反应为:Fe+Ni2O3+3H2O═Fe(OH)2+2Ni(OH)2.下列有关该电池的说法错误的是( )
| A. | 电池的电解液为碱性溶液,负极为Fe | |
| B. | 电池放电时,负极反应为Fe+2OH--2e-═Fe(OH)2 | |
| C. | 电池充电过程中,阴极附近溶液的pH减小 | |
| D. | 电池充电时,OH-向阳极迁移 |
 +H2C=CH2$\stackrel{一定条件}{→}$
+H2C=CH2$\stackrel{一定条件}{→}$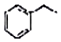
 +2H2C=CH2$\stackrel{一定条件}{→}$
+2H2C=CH2$\stackrel{一定条件}{→}$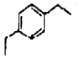
 +2H2C=CH2$\stackrel{一定条件}{→}$
+2H2C=CH2$\stackrel{一定条件}{→}$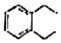
 .
.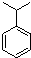 ,N:
,N: .
.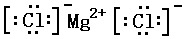 ; ②NaOH
; ②NaOH ;
;