题目内容
14.下列关于硅的说法,不正确的是( )| A. | 硅的化学性质不活泼,常温下不与任何物质反应 | |
| B. | 硅的导电性能介于金属和绝缘体之间,是良好的半导体材料 | |
| C. | 硅是非金属元素,它的单质是灰黑色有金属光泽的固体 | |
| D. | 加热到一定温度时硅能与H2、O2等非金属反应 |
分析 A.硅常温下与氢氟酸、氢氧化钠反应;
B.依据硅的导电性解答;
C.晶体硅的结构与金刚石类似,它是灰黑色有金属光泽的非金属固体;
D.硅与氢气在加热时生成硅烷,与氧气加热生成二氧化硅.
解答 解:A.硅常温下与氢氟酸、氢氧化钠反应,故A错误;
B.硅的导电性能介于金属和绝缘体之间,是良好的半导体材料,故B正确;
C.晶体硅的结构与金刚石类似,它是灰黑色有金属光泽的非金属固体,故C正确;
D.硅与氢气在加热时生成硅烷,与氧气加热生成二氧化硅,所以加热到一定温度时硅能与H2、O2等非金属反应,故D正确;
故选:A.
点评 本题考查了硅的物理性质、化学性质等知识点,难度不大,注意硅常温下、加热条件下能够发生的反应是解题关键,注意对基础知识的积累.

练习册系列答案
相关题目
4.下列说法正确的是( )
| A. | Na、Mg、Al的第一电离能逐渐增大 | B. | V、Cr、Mn的最外层电子数逐渐增大 | ||
| C. | S2-、Cl-、K+的半径逐渐减小 | D. | O、F、Ne的电负性逐渐增大 |
5.根据化合价判断下列加点元素只能表现氧化性的是( )
| A. | H$\underset{\stackrel{\;}{C}}{•}$$\underset{\stackrel{\;}{l}}{•}$ | B. | $\underset{\stackrel{\;}{F}}{•}$$\underset{\stackrel{\;}{e}}{•}$Cl2 | C. | K$\underset{\stackrel{\;}{M}}{•}$$\underset{\stackrel{\;}{n}}{•}$O4 | D. | Na2$\underset{\stackrel{\;}{S}}{•}$O3 |
2.雾霾天气影响着我们的身体健康.下列有关空气污染的说法中,不正确的是( )
| A. | 酸雨的pH<5.6 | |
| B. | SO2、NO2都能引起酸雨 | |
| C. | 雾霾一定是由汽车尾气引起的 | |
| D. | 空气中的SO2主要来自煤、石油的燃烧 |
9.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子. | |
| B. | 硫酸钡难溶于水,但硫酸钡是电解质 | |
| C. | 溶于水后电离出氢离子的化合物都是酸 | |
| D. | 二氧化碳的水溶液能导电,故二氧化碳属于电解质 |
19.运用相关化学知识进行判断,下列结论错误的是( )
| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | NH4F 水溶液中含有 HF,因此 NH4F 溶液不能存放于玻璃试剂瓶中 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成 H2 的速率 |
6.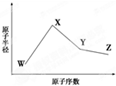 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
Ⅰ.(1)X位于元素周期表中的位置第三周期第ⅠA族;W的基态原子核外有2个未成对电子.
(2)X的单质和Y的单质相比,熔点较高的是Si(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是SiCl4+4H2O=H4SiO4↓+4HCl.
Ⅱ.部分化学键的键能见下表:
(1)比较下列两组物质的熔点高低(填“>”“<”)SiC>Si SiCl4< SiO2
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),计算该反应的反应热△H=+236kJ•mol-1.
 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大.Ⅰ.(1)X位于元素周期表中的位置第三周期第ⅠA族;W的基态原子核外有2个未成对电子.
(2)X的单质和Y的单质相比,熔点较高的是Si(写化学式);Z的气态氢化物和溴化氢相比,较稳定的是HCl(写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是SiCl4+4H2O=H4SiO4↓+4HCl.
Ⅱ.部分化学键的键能见下表:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/ kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
(2)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g),计算该反应的反应热△H=+236kJ•mol-1.
7.下列说法中正确的是( )
| A. | 过氧化氢酶在重金属盐的作用下会失去活性 | |
| B. | 油脂的硬化是指含有不饱和键的油脂发生的催化加氢的反应 | |
| C. | 即使条件不同,卤代烷烃与强碱反应生成的有机物也都只有一种 | |
| D. | 有机物都是由碳、氢和氧三种元素组成的,含有碳元素的物质都是有机物 |