题目内容
19.运用相关化学知识进行判断,下列结论错误的是( )| A. | 某吸热反应能自发进行,因此该反应是熵增反应 | |
| B. | NH4F 水溶液中含有 HF,因此 NH4F 溶液不能存放于玻璃试剂瓶中 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成 H2 的速率 |
分析 A.△H-T△S<0的反应能够自发进行;
B.氟化铵水解生成氟化氢,氢氟酸腐蚀玻璃;
C.海底由天然气与水在高压低温条件下形成的类冰状的结晶物质;
D.常温下铁在浓硫酸中钝化.
解答 解:A.某吸热反应能自发进行,△H>0的反应能够自发进行时,满足△H-T△S<0,△S必须大于0,故A正确;
B.氟化铵水解生成氟化氢,氢氟酸和玻璃中二氧化硅反应腐蚀玻璃,因此NH4F溶液不能存放于玻璃试剂瓶中,故B正确;
C.海底中天然气与水在高压低温条件下形成的类冰状的结晶物质,为可燃冰,存在于海底,故C正确;
D.常温下铁在浓硫酸中钝化,表面形成致密氧化物薄膜阻止浓硫酸与铁反应,不能生成氢气,故D错误;
故选D.
点评 本题考查了物质性质,盐类水解分析应用,注意常温铁在浓硫酸中发生钝化现象,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.20℃时把一定量的20%的某物质的水溶液蒸发10g水后,再冷却到20℃时析出晶体2g(不含结晶水),此时溶液的溶质质量分数为24%,则该物质在20℃时的溶解度为( )
| A. | 20g | B. | 25.4g | C. | 31.6g | D. | 34.8g |
10.下列有关Fe2(SO4)3 溶液的叙述正确的是( )
| A. | 该溶液中,K+、Fe2+、I-、Br-可以大量共存 | |
| B. | 和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 | |
| C. | 1L0.1mol/L该溶液和足量的Cu充分反应,离子方程式为Cu+2Fe3+═Cu2++2Fe2+ | |
| D. | 和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
7.如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( )

| A. | 蒸馏、过滤、分液、蒸发 | B. | 蒸馏、蒸发、分液、过滤 | ||
| C. | 分液、过滤、蒸馏、蒸发 | D. | 过滤、蒸发、分液、蒸馏 |
14.下列关于硅的说法,不正确的是( )
| A. | 硅的化学性质不活泼,常温下不与任何物质反应 | |
| B. | 硅的导电性能介于金属和绝缘体之间,是良好的半导体材料 | |
| C. | 硅是非金属元素,它的单质是灰黑色有金属光泽的固体 | |
| D. | 加热到一定温度时硅能与H2、O2等非金属反应 |
4.在一密闭容器中进行如下反应:3H2(气)+N2(气)?2NH3(气),已知反应过程中某一时 刻 H2、N2、NH3 的浓度分别为 0.3mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是( )
| A. | H2 为 0.6mol/L、N2 为 0.2mol/L | B. | NH3为 0.25mol/L | ||
| C. | N2、NH3 均为 0.15mol/L | D. | NH3为 0.4mol/L |
11.按照碳的骨架分类,下列叙述不正确的是( )
| A. | 碳原子的骨架分类方法一般用于烃的分类 | |
| B. | 五个碳原子的环状化合物肯定是脂环化合物 | |
| C. | 不含苯环的碳环化合物都属于脂环化合物 | |
| D. | 芳香化合物就是指苯及苯的同系物 |
12.某小组为研究电化学原理,设计甲、乙、丙三种装置(C1、C2、C3均为石墨).下列叙述正确的是( )
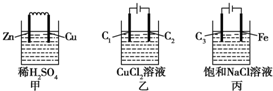

| A. | 甲、丙中是化学能转变为电能,乙中是电能转变为化学能 | |
| B. | C1、C2分别是阳极、阴极,锌片、铁片上都发生氧化反应 | |
| C. | C1上和C3上放出的气体相同,铜片上和铁片上放出的气体也相同 | |
| D. | 甲、乙、丙中溶液的pH都逐渐升高 |