题目内容
20.下列物质属于离子化合物的是( )| A. | CO2 | B. | CaO | C. | H2O2 | D. | H2SO4 |
分析 含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,一般来说,活泼金属和活泼非金属元素之间易形成离子键,铵盐中也含有离子键,只含共价键的化合物是共价化合物,据此分析解答.
解答 解:A.二氧化碳分子中只存在共价键,为共价化合物,故A错误;
B.CaO中钙离子和氧离子之间只存在离子键,为离子化合物,故B正确;
C.双氧水分子中H-O、O-O原子之间只存在共价键,为共价化合物,故C错误;
D.硫酸分子中H-O、O-S原子之间只存在共价键,为共价化合物,故D错误;
故选B.
点评 本题考查离子化合物和共价化合物判断,为高频考点,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,注意双氧水分子中存在的化学键及其空间构型,双氧水是书页型分子结构,题目难度不大.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
10.根据表格中所给的相关数据回答问题
(1)SiCl4的晶体类型是分子晶体;碳化铝的晶体类型是原子晶体.
(2)能否用电解熔融AlCl3的方法来制取铝?为什么?不能(填能或否),理由是AlCl3是分子晶体,熔融时不能导电.
| NaCl | AlCl3 | SiCl4 | 碳化铝 | |
| 熔点 | 810℃ | 190℃ | -68℃ | 2200℃ |
(2)能否用电解熔融AlCl3的方法来制取铝?为什么?不能(填能或否),理由是AlCl3是分子晶体,熔融时不能导电.
8.下列化学反应中,属于氧化还原反应的是( )
| A. | Na2CO3+CaCl2═CaCO3↓+2NaCl | B. | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O | ||
| C. | Fe+CuSO4═Cu+FeSO4 | D. | CaO+H2O═Ca(OH)2 |
12.下列关于Na2CO3和NaHCO3的说法中,不正确的是( )
| A. | 均溶于水 | B. | 受热均易分解 | ||
| C. | 均为钠盐 | D. | 均能与盐酸反应放出CO2 |
9.已知A2On2-可将B2-氧化为B单质,A2On2-则被还原为A3+,又知100mL的0.3mol/L的A2On2-与150mL的0.6mol/L B2-恰好完全反应,则A2On2-中的n值为( )
| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
10.下列叙述正确的是( )
| A. | 某反应的焓变小于零,该反应一定能自发进行 | |
| B. | 用湿润的PH试纸测稀盐酸溶液的pH为3.52 | |
| C. | 原电池是将化学能转变为电能的装置 | |
| D. | 草木灰(K2CO3)是钾肥,硫酸铵是氮肥,两者混合施用可以提高肥效 |
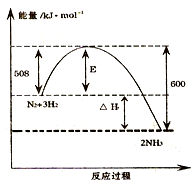 如图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答:
如图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答: 2NH3(g)△H=-92kJ/mol.
2NH3(g)△H=-92kJ/mol.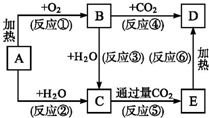 框图中A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.
框图中A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色.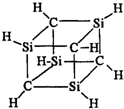 已知化合物A(C4Si4H8)分子结构为正六面体,其结构如图所示:则C4Si4H8的二氯代物的同分异构体数目为( )
已知化合物A(C4Si4H8)分子结构为正六面体,其结构如图所示:则C4Si4H8的二氯代物的同分异构体数目为( )