题目内容
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用如下图所示装置进行有关实验。
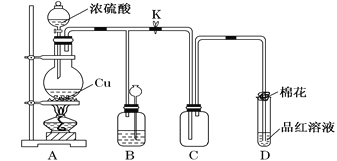
(1)装置A中发生反应的化学方程式为_____________________________________
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是________,其作用是____________________________________________________________________。
(3)装置B的作用是贮存多余的气体。当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是_______________________,B中应放置的溶液是________。
a.水 b.酸性KMnO4溶液
c.浓溴水 d.饱和NaHSO3溶液
(4)实验中,取一定质量的铜片和一定体积18 mol·L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,其原因是____________________________________________________________________。
【答案】 Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑ NaOH 吸收多余的SO2,防止污染空气 广口瓶中液面下降,长颈漏斗液面上升 d 反应过程中浓硫酸被消耗,逐渐变稀,而铜不与稀硫酸反应
CuSO4+2H2O+SO2↑ NaOH 吸收多余的SO2,防止污染空气 广口瓶中液面下降,长颈漏斗液面上升 d 反应过程中浓硫酸被消耗,逐渐变稀,而铜不与稀硫酸反应
【解析】(1)浓硫酸具有强氧化性,在加热时可以氧化单质铜,生成硫酸铜、二氧化硫和水方程式为:Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑;(2)二氧化硫气体排放到大气中污染环境,所以装置D中试管口放置的棉花中应浸一种液体能与二氧化硫反应,可以浸氢氧化钠溶液或碳酸钠溶液等碱性溶液,作用是吸收多余的二氧化硫气体,防止污染空气;(3)置B的作用是贮存多余的气体,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,在密闭容器中随着气体的生成,广口瓶内压强增大,会使瓶内液面下降,长颈漏斗中液面上升,最终达到内外大气压相同,二氧化硫气体是酸性氧化物,易溶于水,B中的试剂不能和二氧化硫发生反应,不能溶解二氧化硫,a.水能溶解二氧化硫不能储存气体,选项a错误;b.酸性KMnO4 溶液能氧化二氧化硫为硫酸,不能储存气体,选项b错误;c.NaOH溶液吸收二氧化硫不能储存气体,选项c错误;d.二氧化硫通入饱和NaHSO3溶液中,降低了二氧化硫的溶解度,不反应,可以用来储存气体,选项d正确;答案选d;(4)一定质量的铜片和一定体积18molL-1的浓硫酸放在圆底烧瓶中共热,浓硫酸随着反应进行,浓度变小成为稀硫酸,稀硫酸不再和铜发生反应,所以有一定量的余酸但未能使用铜片完全溶解,故答案为:随反应进行,硫酸浓度变稀,Cu不与稀H2SO4反应。
CuSO4+2H2O+SO2↑;(2)二氧化硫气体排放到大气中污染环境,所以装置D中试管口放置的棉花中应浸一种液体能与二氧化硫反应,可以浸氢氧化钠溶液或碳酸钠溶液等碱性溶液,作用是吸收多余的二氧化硫气体,防止污染空气;(3)置B的作用是贮存多余的气体,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,在密闭容器中随着气体的生成,广口瓶内压强增大,会使瓶内液面下降,长颈漏斗中液面上升,最终达到内外大气压相同,二氧化硫气体是酸性氧化物,易溶于水,B中的试剂不能和二氧化硫发生反应,不能溶解二氧化硫,a.水能溶解二氧化硫不能储存气体,选项a错误;b.酸性KMnO4 溶液能氧化二氧化硫为硫酸,不能储存气体,选项b错误;c.NaOH溶液吸收二氧化硫不能储存气体,选项c错误;d.二氧化硫通入饱和NaHSO3溶液中,降低了二氧化硫的溶解度,不反应,可以用来储存气体,选项d正确;答案选d;(4)一定质量的铜片和一定体积18molL-1的浓硫酸放在圆底烧瓶中共热,浓硫酸随着反应进行,浓度变小成为稀硫酸,稀硫酸不再和铜发生反应,所以有一定量的余酸但未能使用铜片完全溶解,故答案为:随反应进行,硫酸浓度变稀,Cu不与稀H2SO4反应。

【题目】某待测溶液中可能含有SO42﹣、SO32﹣、CO32﹣、HCO3﹣、NO3﹣、Cl﹣、Br﹣中的若干种及一种常见金属阳离子(Mn+),现进行如下实验(每次实验所用试剂均是足量的,鉴定中某些成分可能没有给出).
请回答下列问题:
(1)根据上述框图信息填写下表(不能确定的不填):
肯定存在的离子 | 肯定没有的离子 | |
化学式或离子符号 |
(2)出沉淀A三种可能的情况: , 若气体D遇空气变红棕色,则生成沉淀D时肯定发生的反应的离子方程式为 .
(3)若Mn+位于第三周期,则要确定它具体是何种离子的方法是 .