题目内容
【题目】短周期主族元素A、B、C、D的原子序数依次增大,其中A、C同主族,B、C、D同周期,A原子的最外层电子数是次外层电子数的3倍,B是短周期元素中原子半径最大的主族元素。试回答下列问题:
(1)A的元素符号__________;D的原子结构示意图_______________。
(2)A、B、C三种元素形成的简单离子的半径由大到小的顺序是(元素符号)__________。
(3)CA2与D元素的单质在水溶液中反应的化学方程式是_____________________。
【答案】 O 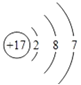 S2->O2->Na+ SO2+Cl2+2H2O=H2SO4+2HCl
S2->O2->Na+ SO2+Cl2+2H2O=H2SO4+2HCl
【解析】短周期主族元素A、B、C、D的原子序数依次增大,A原子的最外层电子数是次外层电子数的3倍,则A为O元素;A、C同主族,C为S元素,D为Cl元素;B、C、D同周期,B是短周期元素中原子半径最大的主族元素,则B为Na元素;则
(1)根据以上分析可知A的元素符号是O;Cl的原子结构示意图为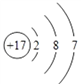 。(2)A、B、C三种元素形成的简单离子O2、Na+、S2-,三种微粒中S2-电子层数最多,故S2-半径最大,O2、Na+电子层数相同,但O2-的核电荷数小,则半径大,故半径由大到小顺序为:S2->O2->Na+;(3)CA2与D元素的单质在水溶液中反应的化学方程式是SO2+Cl2+2H2O=H2SO4+2HCl。
。(2)A、B、C三种元素形成的简单离子O2、Na+、S2-,三种微粒中S2-电子层数最多,故S2-半径最大,O2、Na+电子层数相同,但O2-的核电荷数小,则半径大,故半径由大到小顺序为:S2->O2->Na+;(3)CA2与D元素的单质在水溶液中反应的化学方程式是SO2+Cl2+2H2O=H2SO4+2HCl。

【题目】表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是 , 其离子的原子结构示意图为
(2)写出⑤和⑨最高价氧化物对应水化物间发生反应的离子方程式: .
(3)按要求写出下列两种物质的电子式:①的单质;⑨的过氧化物;
(4)在⑦与⑩的单质中,化学性质较活泼的是 , 可用什么化学反应说明该事实(写出反应的化学方程式): .
(5)请用电子式表示④和⑩组成的化合物的形成过程 .
【题目】下表为元素周期表的一部分。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
1 | ① | ||||||
2 | ② | ⑤ | |||||
3 | ③ | ⑥ | |||||
4 | ④ | ⑦ | |||||
(1)表中元素________(填写元素符号)的非金属性最强;元素________(填写元素符号)的金属性最强,写出它与水反应的离子方程式__________________________________。
(2)表中元素③的原子结构示意图是________。
(3)表中元素⑥、⑦氢化物的稳定性顺序为________>________(填写化学式,下同)。
(4)表中元素最高价氧化物对应水化物酸性最强的酸的分子式是_________________。
【题目】如表所示为自然界中的多种铜矿石的主要成分:
矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3Cu(OH)2 |
请回答:
(1)上表所列铜化合物中,铜的质量百分含量最高的是(填化学式)
(2)工业上以黄铜矿为原料.采用火法溶炼工艺生产铜.该工艺的中间过程包含反应: 2Cu2O+Cu2S ![]() 6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是
6Cu+SO2↑,则该反应的氧化剂与还原剂的物质的量之比是
(3)火法溶炼工艺生产铜的尾气直接排放到大气中造成环境污染的后果是;处理该尾气可得到有价值的化学品,写出其中一种酸和一种盐的名称或化学式、 .
(4)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是(填字母).
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | 铜绿的主成分是碱式碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
C | 铁比铜活泼 | 铆在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |