题目内容
下列离子方程式正确的是( )
| A、漂白粉溶液中通入二氧化硫:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
| B、将0.5molCl2通入含1molFeBr2的溶液中:Cl2+2Fe2+=2Fe3++2Cl- |
| C、碳酸钡中加入稀硫酸:BaCO3+2H+=Ba2++CO2↑+H2O |
| D、水玻璃(硅酸钠水溶液)中滴加稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.次氯酸根具有强的氧化性能够氧化二氧化硫生成硫酸根;
B.二价铁离子的还原性强于溴离子,氯气少量先氧化二价铁离子;
C.硫酸钡为沉淀,保留化学式;
D.硅酸钠是易溶性的盐,应拆成离子形式.
B.二价铁离子的还原性强于溴离子,氯气少量先氧化二价铁离子;
C.硫酸钡为沉淀,保留化学式;
D.硅酸钠是易溶性的盐,应拆成离子形式.
解答:
解:A.漂白粉溶液中通入少量二氧化硫,离子方程式:Ca2++3ClO-+SO2+H2O=Cl-+CaSO4↓+2HClO,故A错误;
B.将0.5molCl2通入含1molFeBr2的溶液中,离子方程式:Cl2+2Fe2+=2Fe3++2Cl-,故B正确;
C.碳酸钡中加入稀硫酸,离子方程式:BaCO3+2H++SO42-=BaSO4↓+H2O+CO2↑,故C错误;
D.水玻璃(硅酸钠水溶液)中滴加稀盐酸,离子方程式:SiO32-+2H+=H2SiO3↓,故D错误;
故选:B.
B.将0.5molCl2通入含1molFeBr2的溶液中,离子方程式:Cl2+2Fe2+=2Fe3++2Cl-,故B正确;
C.碳酸钡中加入稀硫酸,离子方程式:BaCO3+2H++SO42-=BaSO4↓+H2O+CO2↑,故C错误;
D.水玻璃(硅酸钠水溶液)中滴加稀盐酸,离子方程式:SiO32-+2H+=H2SiO3↓,故D错误;
故选:B.
点评:本题考查了离子方程式的正误判断和书写原则,书写时要注意反应的实质、化学式的拆分,题目难度不大.

练习册系列答案
相关题目
如图是一种燃料型电池检测仪的工作原理示意图.下列说法不正确的是( )


| A、该仪器工作时酒精浓度越大,则电流强度越大 |
| B、工作时处电路电子流向为X→Y |
| C、检测结束后,X极区的pH增大 |
| D、电池总反应为2CH3CH2OH+O2═2CH3CHO+2H2O |
下列反应,属于复分解反应的是( )
| A、CaCO3═CaO+CO2↑ |
| B、2HClO═2HCl+O2↑ |
| C、NaOH+HCl═NaCl+H2O |
| D、Fe+CuSO4═FeSO4+Cu |
下列各组中的两种物质作用时,反应条件或反应物的用量比改变,生成的化合物不会改变的是( )
| A、钠与氧气 |
| B、氢氧化钠与二氧化碳 |
| C、过氧化钠与水 |
| D、氯化铝与氢氧化钠 |
下列关于晶体与非晶体的说法不正确的是( )
| A、区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验 |
| B、非晶体中粒子的排列无序,所以非晶体具有各向异性 |
| C、晶体有自范性 |
| D、非晶体无固定熔点 |
化学与生活密切相关,下列说法不正确的是( )
| A、人体内不含消化纤维素的消化酶,因此食物纤维对人体无用 |
| B、碳酸氢钠可用于治疗胃酸过多和焙制糕点 |
| C、油脂从化学成分上讲属于酯类化合物,是人类的主要营养物质之一 |
| D、维生素有20多种,它们多数在人体内不能合成,需要从食物中摄取 |
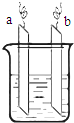 图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag;b极:Fe-2e-=Fe2+下列说法不正确的是( )
图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag;b极:Fe-2e-=Fe2+下列说法不正确的是( )| A、a、b可能是同种电极材料 |
| B、该装置一定是电解池 |
| C、装置中电解质溶液一定含有Ag+ |
| D、装置中发生的反应方程式一定是Fe+2Ag+═Fe2++2Ag |
下列说法中正确的是(NA表示阿伏加德罗常数的值)( )
| A、在常温常压下,11.2L N2含有的分子数为0.5NA |
| B、在常温常压下,1mol H2含有的原子数为2NA |
| C、71g Cl2的体积约为22.4L |
| D、在同温同压下,相同体积的任何气体单质所含的原子数相同 |