题目内容
NA代表阿伏加德罗常数.下列有关NA的叙述中,正确的是( )
| A、1mol任何物质所含的分子数均为NA |
| B、14g氮气所含的氮原子数为NA |
| C、标准状况下,22.4L水所含的水分子数为NA |
| D、在钠与氯气的反应中,1mol钠失去电子的数目为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.有的物质中不存在分子,如离子晶体、原子晶体、金属晶体等;
B.14g氮气中含有14g氮原子,含有1mol氮原子;
C.标准状况下,水的状态不是气体,不能使用气体摩尔体积计算其物质的量;
D.钠为+1价金属,1mol钠完全反应失去1mol电子.
B.14g氮气中含有14g氮原子,含有1mol氮原子;
C.标准状况下,水的状态不是气体,不能使用气体摩尔体积计算其物质的量;
D.钠为+1价金属,1mol钠完全反应失去1mol电子.
解答:
解:A.由于离子晶体、原子晶体、金属晶体中不存在分子,故A错误;
B.14g氮气中含有氮原子的物质的量为:
=1mol,所含的氮原子数为NA,故B正确;
C.标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量,故C错误;
D.1mol钠完全反应最多失去1mol电子,失去电子的数目为NA,故D错误;
故选B.
B.14g氮气中含有氮原子的物质的量为:
| 14g |
| 14g/mol |
C.标况下水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量,故C错误;
D.1mol钠完全反应最多失去1mol电子,失去电子的数目为NA,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的应用,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各物质分别滴加浓硫酸后,现象描述正确的是( )
| A、胆矾晶体由蓝色变无色 |
| B、pH试纸变红 |
| C、蓝色石蕊试液褪色 |
| D、白纸变黑 |
下列关于金属腐蚀的叙述不正确的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、与生铁相比纯铁更容易被腐蚀 |
| C、金属的吸氧腐蚀和析氢腐蚀都属于电化学腐蚀 |
| D、金属腐蚀的本质是M-ne?=Mn+ |
雌黄与浓硝酸反应如下:As2S3+28HNO3(浓)?2H3As04+3H2S04+28N02↑+8H2O,下列说法正确的是( )
| A、氧化产物只有H2S04 |
| B、1mol As2S3发生反应,有28 mol电子转移 |
| C、该反应中As2S3既是氧化剂又是还原剂 |
| D、As2S3不可能与氧气反应 |
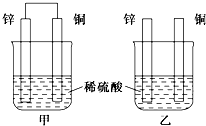 将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题: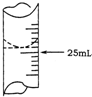 欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).
欲测定某NaOH溶液的物质的量浓度,可用物质的量浓度为0.1000mol?L-1 HCl标准溶液进行中和滴定(用酚酞作指示剂).