题目内容
12.如表是元素周期表的一部分,回答下列有关问题:| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
 ①的气态氢化物的电子式
①的气态氢化物的电子式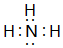 .
.(2)写出⑪元素基态原子的价电子排布式4s2.
(3)在这些元素的最高价氧化物对应水化物中,有一种呈两性的用来治疗胃酸过多反应的离子方程式:Al(OH)3+3H+=Al3++3H2O.
(4)在这些元素中,某元素的最高价氧化物对应的水化物可以和其气态氢化物反应,写出该反应化学方程式NH3+HNO3=NH4NO3或 2H2S+H2SO4(浓)=3H2O+2S+SO2.
(5)如何证明元素⑦与⑧的非金属性强弱,写出可以验证该结论的一个离子反应方程式S2-+Cl2=S↓+2Cl-.
(6)在这些元素中VIIA氢化物的稳定性由强到弱HF>HCl>HBr(用化学式作答)
分析 由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为S,⑧为Cl,⑨为Ar,⑩为K,⑪为Ca,⑫为Br.
(1)元素②为F,离子核外电子数为10,各层电子数为2、8;①的气态氢化物为NH3;
(2)⑪处于第四周期IIA族,价电子为4s电子;
(3)最高价氧化物对应水化物中,呈两性的用来治疗胃酸过多为氢氧化铝,胃酸主要为盐酸,二者反应生成氯化铝与水;
(4)某元素的最高价氧化物对应的水化物可以和其气态氢化物反应,可以是氨气与硝酸反应生成硝酸铵,或者硫化氢与浓硫酸反应生成硫与水;
(5)可以利用单质之间相互置换反应证明元素非金属性强弱;
(6)非金属性越强,对应氢化物越稳定.
解答 解:由元素在周期表中的位置可知,①为N,②为F,③为Na,④为Mg,⑤为Al,⑥为Si,⑦为S,⑧为Cl,⑨为Ar,⑩为K,⑪为Ca,⑫为Br.
(1)元素②为F,离子核外电子数为10,离子结构示意图为 ;①的气态氢化物为NH3,电子式为
;①的气态氢化物为NH3,电子式为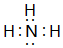 ,
,
故答案为: ;
;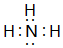 ;
;
(2)⑪处于第四周期IIA族,价电子为4s电子,价电子排布式为:4s2,
故答案为:4s2;
(3)最高价氧化物对应水化物中,呈两性的用来治疗胃酸过多为氢氧化铝,胃酸主要为盐酸,二者反应生成氯化铝与水,反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;
(4)某元素的最高价氧化物对应的水化物可以和其气态氢化物反应,可以是氨气与硝酸反应生成硝酸铵,或者硫化氢与浓硫酸反应生成硫与水,反应方程式为:NH3+HNO3=NH4NO3或 2H2S+H2SO4(浓)=3H2O+2S+SO2,
故答案为:NH3+HNO3=NH4NO3或 2H2S+H2SO4(浓)=3H2O+2S+SO2;
(5)可以利用单质之间相互置换反应证明元素非金属性强弱,反应离子方程式为:S2-+Cl2=S↓+2Cl-,
故答案为:S2-+Cl2=S↓+2Cl-;
(6)同主族自上而下非金属性减弱,非金属性越强,对应氢化物越稳定,故氢化物稳定性:HF>HCl>HBr,
故答案为:HF>HCl>HBr.
点评 本题考查元素周期表与元素周期律应用、常用化学用语、元素化合物知识,注意掌握金属性、非金属性强弱比较实验事实.

| A. | 铝粉投入到冷浓硝酸中:2Al+6H+=2Al3++3H2↑ | |
| B. | 铁与盐酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 用小苏打治疗胃酸过多:H++HCO3-=H2O+CO2↑ | |
| D. | Ba(OH)2与稀H2SO4反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| 甲的球棍模型 | 乙的结构式 | 丙的球棍模型 | 丁的比例模型 |
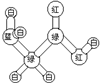 | 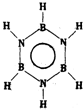 | 丙的分子式为C13H10O3 | 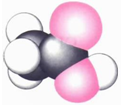 |
下列叙述不正确的是( )
| A. | 甲可代表氨基酸 | B. | 乙的二氯代物有3种 | ||
| C. | 丙的结构简式为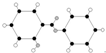 | D. | 丁可代表乙酸 |
| A. | 石油 | B. | 农作物秸秆 | C. | 煤 | D. | 氢气 |
| A. | 大力发展以煤炭为原料的火力发电,促进经济发展 | |
| B. | 在生产和生活中提倡使用节能技术和节能用具 | |
| C. | 开发新能源,代替传统能源 | |
| D. | 提倡乘坐公交车、骑自行车或步行的方式出行 |
| A. | 2-甲基-氯丙烷 | B. | 2-甲基-3-丁烯 | ||
| C. |  1,3,4-三甲苯 1,3,4-三甲苯 | D. | 2,3-二甲基-4-乙基己烷 |
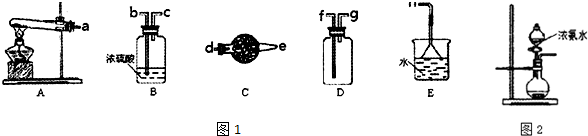
 .
.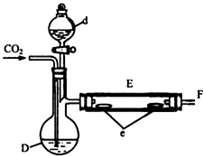 实验室用如图所示装置制取溴化亚铁.D和d中均盛有液溴,E为外套电炉丝的瓷管,e是两只耐高温的瓷皿,其中共盛有56g细铁粉.实验开始时先将干燥、纯净的CO2气流通入D中,然后将铁粉加热至600℃~700℃,E管中反应开始.E中的反应为:2Fe+3Br2═2FeBr3,2FeBr3$\frac{\underline{\;\;△\;\;}}{\;}$2FeBr2+Br2↑,最后将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁80g.请回答:
实验室用如图所示装置制取溴化亚铁.D和d中均盛有液溴,E为外套电炉丝的瓷管,e是两只耐高温的瓷皿,其中共盛有56g细铁粉.实验开始时先将干燥、纯净的CO2气流通入D中,然后将铁粉加热至600℃~700℃,E管中反应开始.E中的反应为:2Fe+3Br2═2FeBr3,2FeBr3$\frac{\underline{\;\;△\;\;}}{\;}$2FeBr2+Br2↑,最后将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁80g.请回答: