题目内容
6.图甲为一种新型污水处理装置,该装置可利用一种微生物将有机废水的化学能直接转化为电能.图乙为电解氯化铜溶液的实验装置的一部分.下列说法中正确的是( )
| A. | a极要与Y极连接 | |
| B. | N电极发生还原反应,当N电极消耗5.6L(标准状况下)气体时,则a电极增重64g | |
| C. | 不论b为何种电极材料,b极的电极反应式一定为2C1--2e-=Cl2↑ | |
| D. | 若有机废水中主要含有乙醛,则图甲中M极发生的电极应为:CH3CHO+3H2O-l0e-=2CO2↑+l0H+ |
分析 根据题给信息知,甲图是将化学能转化为电能的原电池,M是负极,N是正极,负极上失电子发生氧化反应,正极上得电子发生还原反应,电解氯化铜溶液,由图乙氯离子移向b极,铜离子移向a极,则a为阴极应与负极相连,b为阳极应与正极相连,根据得失电子守恒计算,以此解答该题.
解答 解:A.根据以上分析,M是负极,N是正极,a为阴极应与负极相连即X极连接,故A错误;
B.N是正极氧气得电子发生还原反应,a为阴极铜离子得电子发生还原反应,根据得失电子守恒,则当N电极消耗5.6L(标准状况下)气体时,则a电极增重$\frac{5.6L}{22.4L/mol}$×$\frac{4}{2}$×64g/mol=32g,故B错误;
C.b为阳极,当为惰性电极,则反应式为2C1--2e-=Cl2↑,当为活性电极,反应式为本身失电子发生氧化反应,故C错误;
D.有机废水中主要含有乙醛,则图甲中M极为CH3CHO失电子发生氧化反应,发生的电极应为:CH3CHO+3H2O-l0e-=2CO2↑+l0H+,故D正确.
故选D.
点评 本题考查了原电池原理以及电镀原理,为高频考点,侧重于学生的分析、计算能力的考查,明确原电池正负极上得失电子、电解质溶液中阴阳离子移动方向即可解答,难度中等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
17.下列叙述正确的是( )

| A. | 将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 | |
| B. | 将一小块钠放入盛有水的烧杯中,钠在水面上游动,同时看到烧杯内的溶液变为红色 | |
| C. | 向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 | |
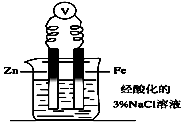
| D. | 向图中烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,一段时间后可看到Fe电极附近有蓝色沉淀生成 |
1.下列化合物属于混合物的是( )
| A. | 纤维素 | B. | 氯乙烯 | C. | 冰醋酸 | D. | 乙酸乙酯 |
17.10L 1mol/L Al2(SO4)3溶液中含有SO${\;}_{4}^{2-}$的物质的量浓度是( )
| A. | 1mol/L | B. | 2mol/L | C. | 3mol/L | D. | 20mol/L |
 2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为,用O2浓度变化来表示的反应速率为。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
2SO3,如果2min内SO2的浓度由6mol/L下降为2mol/L,那么,用SO2浓度变化来表示的化学反应速率为,用O2浓度变化来表示的反应速率为。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L·min),那么2min时SO2的浓度为 。
 .
. 2SO3,下列哪个量不再变化时,并不能说明化学反应已达到平衡状态( )
2SO3,下列哪个量不再变化时,并不能说明化学反应已达到平衡状态( ) 4NO+6H2O,下述化学反应速率关系表述正确的是( )
4NO+6H2O,下述化学反应速率关系表述正确的是( )