题目内容
13.分子式为C4H6O5的有机物A有如下性质( )①1mol A+2mol NaOH→正盐,②A+RCOOH或ROH$\stackrel{一定条件}{→}$有香味的物质(R为烃基),③1mol A$\stackrel{足量Na}{→}$1.5mol气体,④A的分子内脱水产物(不是环状化合物)可使溴水褪色.
根据以上信息,对A的结构判断错误的是( )
| A. | 肯定没有碳碳双键 | B. | 有两个羧基 | ||
| C. | 肯定有醇羟基 | D. | 有RCOOR'结构 |
分析 由②A+RCOOH或ROH$\stackrel{一定条件}{→}$有香味的物质(R为烃基)可知有机物含有羟基和羧基;由①1mol A+2mol NaOH→正盐可知有机物含有2个羧基,由③1mol A$\stackrel{足量Na}{→}$1.5mol气体可知含有1个羟基,由④A的分子内脱水产物(不是环状化合物)可使溴水褪色可知有机物可发生消去反应,以此解答该题.
解答 解:由②A+RCOOH或ROH$\stackrel{一定条件}{→}$有香味的物质(R为烃基)可知有机物含有羟基和羧基;由①1mol A+2mol NaOH→正盐可知有机物含有2个羧基,由③1mol A$\stackrel{足量Na}{→}$1.5mol气体可知含有1个羟基,由④A的分子内脱水产物(不是环状化合物)可使溴水褪色可知有机物可发生消去反应,结构为HOOC-CHOH-CH2-COOH.
故选D.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能力的考查,明确物质含有的官能团及其性质是解本题关键,难度不大.

练习册系列答案
相关题目
6.下列反应属于取代反应的是( )
| A. | 由乙酸和乙醇制乙酸乙酯 | B. | 由乙醇制乙烯 | ||
| C. | 由丙烯与溴制1,2-二溴丙烷 | D. | 由甲苯氧化制苯甲酸 |
4.下列各组离子,能在水溶液中大量共存的是( )
| A. | Na+、Ba2+、SO42-、Cl- | B. | Mg2+、K+、Cl-、NO3- | ||
| C. | H+、K+、CO32-、NO3- | D. | Ag+、Ca2+、Cl-、HCO3- |
1.利用如图装置制取溴苯,下列说法不正确的是( )


| A. | 该装置中CCl4的作用是除去产物HBr中混有的Br2蒸气 | |
| B. | 若将液溴改为浓溴水,该反应也能进行 | |
| C. | 通过AgNO3溶液中有淡黄色沉淀产生,说明由苯制溴苯的反应是取代反应 | |
| D. | 该装置中左侧长导管的作用是导气兼冷凝回流 |
8.下列化学用语中,正确的是( )
| A. | 氯化钠的电子式为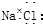 ? ? | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 氯化氢分子的形成过程可用电子式表示为:H×+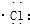 → →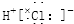 | |
| D. | 重水的化学式为${\;}_{1}^{2}$H2O(或D2O) |
18.课外实验小组为了探究锌与盐酸反应过程中的化学反应速率的变化,在100mL稀盐酸中加入足量的锌粉,标准状况下用排水集气法收集反应放出的氢气,实验记录如下(累计值):
(1)哪一时间段2~3 min(指0~1、1~2、2~3、3~4、4~5min,下同)反应速率最大,可能的原因是该反应是放热反应,此时温度高.
(2)哪一段时段的反应速率最小4~5min,原因是H+浓度小.
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率为0.1mol/(L•min).
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.蒸馏水B.CH3COONa固体 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是AB(填编号).
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
(2)哪一段时段的反应速率最小4~5min,原因是H+浓度小.
(3)求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率为0.1mol/(L•min).
(4)如果反应太激烈,为了减缓反应速率而又不减少产生氢气的量,在盐酸中分别加入下列物质:
A.蒸馏水B.CH3COONa固体 C.Na2CO3溶液 D.CuSO4溶液
你认为可行的是AB(填编号).
2.下列电离方程式正确的是( )
| A. | Al2(SO4)3═2Al3++3SO42- | B. | NaHCO3═Na++H++CO32- | ||
| C. | Ba(OH)2═Ba2++(OH-)2 | D. | Na2SO3═Na++SO32- |
20.下列各图所示装置属于原电池的是( )
| A. |  | B. |  | C. |  | D. |  |

 .
. .F1和F2的关系为同分异构体.
.F1和F2的关系为同分异构体. ,二烯烃的通式是CnH2n-2.
,二烯烃的通式是CnH2n-2.