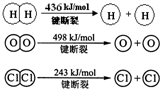
题目内容
(1)写出下列微粒的电子式.
C2H4 ;CH3- ;OH- .
(2)键线式 表示的分子式 ;结构简式为 ;名称是 .
表示的分子式 ;结构简式为 ;名称是 .
(3)根据命名写出该物质的结构简式:
2,3-二甲基-2-戊烯 ;对二甲苯 .
C2H4
(2)键线式
 表示的分子式
表示的分子式(3)根据命名写出该物质的结构简式:
2,3-二甲基-2-戊烯
考点:电子式、化学式或化学符号及名称的综合,有机化合物命名
专题:有机化学基础
分析:(1)乙烯分子中存在碳碳双键、甲基中含有3个碳氢键、氢氧根离子为阴离子,据此书写出各物质的电子式;
(2)根据键线式写出该有机物的结构简式、分子式,然后根据烷烃的命名原则对该有机物命名;
(3)根据烷烃的命名原则写出该有机物的结构简式.
(2)根据键线式写出该有机物的结构简式、分子式,然后根据烷烃的命名原则对该有机物命名;
(3)根据烷烃的命名原则写出该有机物的结构简式.
解答:
解:(1)烯的分子式为C2H4,分子中碳原子与碳原子通过两对共用电子对相连接,碳原子与氢原子通过一对共用电子对相连接,所以电子式为: ;
;
甲基中碳原子最外层为7个电子,甲基的电子式为: ;
;
氢氧根离子为带有1个单位负电荷的阴离子,需要标出离子中各原子最外层电子,氢氧根离子的电子式为: ;
;
故答案为: ;
; ;
; ;
;
(2) 的结构简式为:(CH3)2CH(CH2)2CH3,该有机物分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,该有机物命名为:2-甲基戊烷,
的结构简式为:(CH3)2CH(CH2)2CH3,该有机物分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,该有机物命名为:2-甲基戊烷,
故答案为:C6H14;(CH3)2CH(CH2)2CH3; 2-甲基戊烷;
(3)2,3-二甲基-2-戊烯:该有机物主链为2-戊烯,碳碳双键在2号C,在2、3号C各含有1个甲基,该有机物结构简式为:(CH3)2C=C(CH3)CH2CH3;
对二甲苯:在苯环的对位碳原子上含有两个甲基,其结构简式为: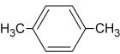 ,
,
故答案为:(CH3)2C=C(CH3)CH2CH3; .
.
 ;
;甲基中碳原子最外层为7个电子,甲基的电子式为:
 ;
;氢氧根离子为带有1个单位负电荷的阴离子,需要标出离子中各原子最外层电子,氢氧根离子的电子式为:
 ;
;故答案为:
 ;
; ;
; ;
;(2)
 的结构简式为:(CH3)2CH(CH2)2CH3,该有机物分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,该有机物命名为:2-甲基戊烷,
的结构简式为:(CH3)2CH(CH2)2CH3,该有机物分子中含有6个碳原子,属于饱和烃,分子式为C6H14,该有机物主链上有5个C,2号C一个甲基,该有机物命名为:2-甲基戊烷,故答案为:C6H14;(CH3)2CH(CH2)2CH3; 2-甲基戊烷;
(3)2,3-二甲基-2-戊烯:该有机物主链为2-戊烯,碳碳双键在2号C,在2、3号C各含有1个甲基,该有机物结构简式为:(CH3)2C=C(CH3)CH2CH3;
对二甲苯:在苯环的对位碳原子上含有两个甲基,其结构简式为:
 ,
,故答案为:(CH3)2C=C(CH3)CH2CH3;
 .
.
点评:本题考查了电子式、有机物命名及结构简式的书写,题目难度不大,注意掌握常见有机物结构及命名原则,明确电子式的书写原则,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
25C 时,下列溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1mol?L-1 pH为4的NaHB溶液中,c(HB-)>c(H2B)>c(B2-) |
| B、0.4mol?L-1 NH4Cl和0.2mol?L-1 NaOH两种溶液等体积混合后pH=9:c(NH4+)>c(Cl-)>c(Na+)>c(OH-)>c(H+) |
| C、pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(NaOH)<c(Na2CO3)<c(CH3COONa) |
| D、在0.1mol/L CH3COONa溶液中:c(H+)=c(CH3COOH)+c(OH-) |
在核磁共振氢谱中出现三组峰的化合物是( )
A、 |
B、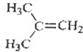 |
C、 |
D、 |