题目内容
生铁中一般含有化合物B,B只有两种元素组成,它的含量、形状、分布对生铁性能影响很大,使生铁硬而脆,不宜进行机械加工.
已知:
(1)E、F、H、I、P常温下为气体,H、l、P为单质,E是一种红棕色气体.
(2)反应①②均为制备理想的绿色水处理剂Na2FeO4的方法,其中反应①在生成Na2FeO4同时还生成NaNO2和H2O.各物质之闻的转化关系如图所示f图中部分生成物没有列出).

请填写以下空白:
(1)用电子式表示F的形成过程
(2)按要求完成下列反应:反应③的离子方程式为 反应①的化学方程式为
(3)反应②中氧化剂与还原剂的物质的量比为 反应④中的氧化产物的化学式为
(4)实验室中检验C溶液中金属阳离子的常用方法是
(5)如果A与B反应时生成E与F的物质的量比为13:1,则化合物B的化学式为 .
已知:
(1)E、F、H、I、P常温下为气体,H、l、P为单质,E是一种红棕色气体.
(2)反应①②均为制备理想的绿色水处理剂Na2FeO4的方法,其中反应①在生成Na2FeO4同时还生成NaNO2和H2O.各物质之闻的转化关系如图所示f图中部分生成物没有列出).

请填写以下空白:
(1)用电子式表示F的形成过程
(2)按要求完成下列反应:反应③的离子方程式为
(3)反应②中氧化剂与还原剂的物质的量比为
(4)实验室中检验C溶液中金属阳离子的常用方法是
(5)如果A与B反应时生成E与F的物质的量比为13:1,则化合物B的化学式为
考点:无机物的推断
专题:推断题
分析:由流程转化图可知,常温下F为气体且和过氧化钠反应生成单质H,则H为O2,F为CO2,N为Fe2O3,红棕色气体E为NO2,应是氧化性酸HNO3的还原产物,推断A可能是浓HNO3,生铁中一般含有化合物B,B只有两种元素组成,它的含量、形状、分布对生铁性能影响很大,使生铁硬而脆,不宜进行机械加工,化合物B应是碳元素和铁元素组成的,和硝酸发生氧化还原反应,依据E+D+H=A判断D为H2O,C可能为Fe(NO3)2或Fe(NO3)3,G和D混合电解生成单质PI和J,J和A反应生成D和K,说明J为碱性溶液,证明G为NaCl,J为NaOH,I为Cl2,P为H2,K为KNO3,I+J=D+L+G分析可知,L为NaClO,C+J=M,则M为Fe(OH)3,据此推断回答问题.
解答:
解:由流程转化图可知,常温下F为气体且和过氧化钠反应生成单质H,则H为O2,F为CO2,N为Fe2O3,红棕色气体E为NO2,应是氧化性酸HNO3的还原产物,推断A可能是浓HNO3,生铁中一般含有化合物B,B只有两种元素组成,它的含量、形状、分布对生铁性能影响很大,使生铁硬而脆,不宜进行机械加工,化合物B应是碳元素和铁元素组成的,和硝酸发生氧化还原反应,依据E+D+H=A判断D为H2O,C可能为Fe(NO3)2或Fe(NO3)3,G和D混合电解生成单质PI和J,J和A反应生成D和K,说明J为碱性溶液,证明G为NaCl,J为NaOH,I为Cl2,P为H2,K为KNO3,I+J=D+L+G分析可知,L为NaClO,C+J=M,则M为Fe(OH)3,C为Fe(NO3)3;
(1)二氧化碳为共价化合物,根据共价化合物电子式的表示方法用电子式表示出CO2的形成过程,二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,形成过程为: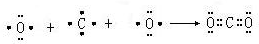 ,
,
故答案为: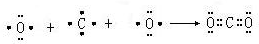 ;
;
(2)反应③是电解饱和食盐水,反应的离子方程式为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;反应①是氢氧化钠和硝酸钠和氧化铁反应生成高铁酸钠、亚硝酸钠和水,反应的化学方程式为4NaOH+3NaNO3+Fe2O3=2Na2FeO4+3NaNO2+2H2O;
故答案为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;4NaOH+3NaNO3+Fe2O3=2Na2FeO4+3NaNO2+2H2O;
(3)反应②是氢氧化铁和次氯酸钠、氢氧化钠反应生成高铁酸钠、氯化钠和水,反应的化学方程式为:4NaOH+2Fe(OH)3+3NaClO=2Na2FeO4+3NaCl+5H2O,依据元素化合价变化分析反应中氧化剂为NaClO与还原剂Fe(OH)3的物质的量比为3:2,反应④是FeS2和氧气反应生成氧化铁和二氧化硫,2FeS2+11O2
Fe2O3+8SO2,氧化产物的化学式为Fe2O3 SO2 ;
故答案为:3:2;Fe2O3 SO2 ;
(4)实验室中检验C溶液中金属阳离子的常用方法是,取适量C溶液于试管中,滴加少量KSCN溶液,溶液变红色,说明C溶液中金属阳离子为Fe3+;
故答案为:取适量C溶液于试管中,滴加少量KSCN溶液,溶液变红色,说明C溶液中金属阳离子为Fe3+;
(5)如果A与B反应时生成E为NO2与F为CO2的物质的量比为13:1,依据电子守恒分析,设碳元素化合价为x
HNO3~NO2~e-
C~CO2~(4-x)e-
(4-x)=13,x=-9;
则B为Fe3C;
故答案为:Fe3C.
(1)二氧化碳为共价化合物,根据共价化合物电子式的表示方法用电子式表示出CO2的形成过程,二氧化碳是氧原子和碳原子之间通过共价键形成的共价化合物,形成过程为:
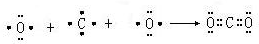 ,
,故答案为:
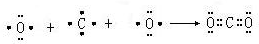 ;
;(2)反应③是电解饱和食盐水,反应的离子方程式为:2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
(3)反应②是氢氧化铁和次氯酸钠、氢氧化钠反应生成高铁酸钠、氯化钠和水,反应的化学方程式为:4NaOH+2Fe(OH)3+3NaClO=2Na2FeO4+3NaCl+5H2O,依据元素化合价变化分析反应中氧化剂为NaClO与还原剂Fe(OH)3的物质的量比为3:2,反应④是FeS2和氧气反应生成氧化铁和二氧化硫,2FeS2+11O2
| ||
故答案为:3:2;Fe2O3 SO2 ;
(4)实验室中检验C溶液中金属阳离子的常用方法是,取适量C溶液于试管中,滴加少量KSCN溶液,溶液变红色,说明C溶液中金属阳离子为Fe3+;
故答案为:取适量C溶液于试管中,滴加少量KSCN溶液,溶液变红色,说明C溶液中金属阳离子为Fe3+;
(5)如果A与B反应时生成E为NO2与F为CO2的物质的量比为13:1,依据电子守恒分析,设碳元素化合价为x
HNO3~NO2~e-
C~CO2~(4-x)e-
(4-x)=13,x=-9;
则B为Fe3C;
故答案为:Fe3C.
点评:本题考查了物质转化关系的分析,物质性质的理解应用,主要是铁及其化合物性质的应用,高铁酸钠的制备原理是关键,题目难度较大.

练习册系列答案
相关题目
包装危险时,常贴上一些图标用来提醒人们.下列是一些常见危险品的图标,装运酒精时应贴的图标是( )
A、. 易燃性 |
B、 爆炸性 |
C、. 有毒性 |
D、. 腐蚀性 |
 表示的分子式
表示的分子式
 金属冶炼与处理常涉及氧化还原反应
金属冶炼与处理常涉及氧化还原反应