题目内容
3.在下列条件下,可能大量共存的离子组是( )| A. | c(H+)=1×10-14mol/L的溶液:K+、Cu2+、I-、SO42- | |
| B. | 水电离出的c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- | |
| C. | 能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- | |
| D. | 能与K3[Fe(CN)6]产生蓝色沉淀的溶液:H+、Na+、SO42-、CrO42- |
分析 A.该溶液中存在大量氢氧根离子,铜离子与氢氧根离子反应;
B.水电离出的c(H+)=1×10-14mol/L的溶液中存在大量氢离子或氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
C.能与Al反应生成H2的溶液中存在大量氢离子或氢氧根离子,铵根离子与氢氧根离子反应,硝酸根离子在酸性条件下能够氧化碘离子;
D.能与K3[Fe(CN)6]产生蓝色沉淀的溶液中存在亚铁离子,CrO42-在酸性条件下能够氧化亚铁离子.
解答 解:A.c(H+)=1×10-14mol/L的溶液中存在大量氢氧根离子,Cu2+与氢氧根离子反应,在溶液中不能大量共存,故A错误;
B.该溶液呈酸性或碱性,溶液中存在大量氢离子或氢氧根离子,K+、Na+、AlO2-、S2O32-之间不反应,都不与氢氧根离子反应,在碱性溶液中能够大量共存,故B正确;
C.能与Al反应生成H2的溶液层酸性或碱性,NH4+与碱性溶液中的氢氧根离子反应,NO3-、I-在酸性条件下发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.Fe2+和K3[Fe(CN)6]溶液反应生成特征蓝色沉淀,说明溶液中含有亚铁离子,CrO42-在酸性条件下能够氧化亚铁离子,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存,为高考的高频题,题目难度不大,注意掌握离子不能大量共存的一般情况:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等;试题侧重对学生基础知识的训练和检验,有利于培养学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
13.将100g溶质质量分数为w1,物质的量浓度为c1的浓硫酸沿玻璃棒加入到Vml水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀溶液.下列说法中正确的是( )
| A. | 若c1=2c2,则w1<2w2,V<100mL | B. | 若c1=2c2,则w1>2w2,V>100mL | ||
| C. | 若w1=2w2,则c1>2c2,V=100mL | D. | 若w1=2w2,则c1>2c2,V<100mL |
14.下列气体中,能使品红溶液褪色的是( )
| A. | N2 | B. | CO2 | C. | SO2 | D. | CH4 |
11.下列有关金属的说法正确的是( )
| A. | 湿法炼铜和火法炼铜的反应中,铜元素都发生还原反应 | |
| B. | 加强热,使CuO在高温条件下分解制备单质Cu | |
| C. | 黑色金属材料包括铁、铬、锰及其化合物 | |
| D. | 生铁与钢的区别在于生铁含碳杂质,而钢不含 |
18.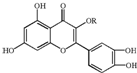 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )| A. | 分子中的官能团有羟基、碳碳双键、醚键、酯基 | |
| B. | 若R为乙基则该物质的分子式可以表示为C16H14O7 | |
| C. | lmol该化合物最多可与7mol Br2完全反应 | |
| D. | lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol |
8.可逆反应:N2(g)+3H2(g)?2NH3(g)的正逆反应速率可用反应物或生成物的浓度变化来表示,下列各关系中能说明反应已达平衡状态的是( )
| A. | v正(N2)=v正(H2) | B. | v正(N2)=v逆(NH3) | ||
| C. | 2 v正(H2)=3 v逆(NH3) | D. | v正(N2)=v逆(H2) |