题目内容
20.某有机物的结构简式为 ,关于该物质的叙述正确的是( )
,关于该物质的叙述正确的是( )| A. | 该物质不能使酸性KMnO4溶液褪色 | |
| B. | 该物质的一氯代物有6种 | |
| C. | 1mol该物质与足量的H2反应,消耗H2的物质的量为5 mol | |
| D. | 1 mol该物质与足量的NaOH溶液反应,消耗NaOH的物质的量为2mol |
分析 由结构可知,分子中含-COOC-,苯环上还有3个H,除甲基外的2个取代基不同,甲基能被强氧化剂氧化,以此来解答.
解答 解:A.与苯环直接相连的是甲基,可被酸性高锰酸钾氧化为羧基,酸性KMnO4溶液褪色,故A错误;
B.结构不对称,则苯环上的一氯代物有3种,三个取代基分被各有一种一氯代物,该物质的一氯代物有6种,故B正确;
C.该结构中只有苯环能与氢气加成,1mpl苯环完全加成消耗3mol氢气,故C错误;
D.1 mol该物质中含有2mol酯基,但是有1mol酯基与苯环直接相连的是O,水解后消耗2mol氢氧化钠,另1mol酯基消耗1mol氢氧化钠,与足量的NaOH溶液反应共消耗3mol氢氧化钠,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重有机物性质及分析与应用能力的考查,题目难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
19.下列混合物,不论它们按何种比例混合,只要质量一定,经完全燃烧后产生的CO2和H2O的物质的量均为常数的是( )
| A. | 乙炔和苯 | B. | 甲烷和乙烷 | C. | 乙烯和丁炔 | D. | 苯和苯乙烯 |
11.短周期元素A、B、C、D最高价氧化物对应水化物分别为W、X、Y、Z,A是短周期中原子半径最大的元素,常温下W、Y、Z均可与X反应,A、C、D的原子序数及0.1mol/L W、Y、Z溶液的pH如图所示(已知lg2=0.3).下列说法正确的是( )

| A. | B的离子半径大于A的离子半径 | |
| B. | C氢化物稳定性大于D氢化物稳定性 | |
| C. | W、Z两物质含有的化学键类型相同 | |
| D. | B原子的电子层数与最外层电子数相等 |
15.现有①石油的分馏 ②煤的干馏 ③油脂的硬化 ④蛋白质的盐析⑤蛋白质的变性 ⑥橡胶的老化 ⑦油脂的皂化.其中属于物理变化的是( )
| A. | ①②④⑦ | B. | ①④ | C. | ③④⑥ | D. | ①③⑥ |
12.在恒容条件下,能使反应NO2 (g)+CO(g)?NO(g)+CO2(g)的反应速率增大且活化分子的百分数也增大的措施是( )
| A. | 增大 NO2或CO的浓度 | B. | 减小 NO或CO2的浓度 | ||
| C. | 通入Ne使气体的压强增大 | D. | 升高反应温度 |
9.设NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 标准状况下,2.24LSO3所含分子数为0.1NA | |
| B. | 0.1 mol Fe与足量盐酸反应,转移的电子数为0.3 NA | |
| C. | 1molNa2O2与足量水反应转移的电子数为NA | |
| D. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA |
10.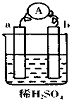 在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述正确的是( )
在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述正确的是( )
 在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述正确的是( )
在如图所示的装置中,a的金属性比氢要强,b为碳棒,关于此装置的各种叙述正确的是( )| A. | 碳棒上有气体放出,溶液pH变小 | B. | a是正极,b是负极 | ||
| C. | 溶液中阳离子移向a极 | D. | a极上发生了氧化反应 |
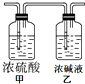 某有机物X相对氢气的密度为30,9g该有机物在空气中充分燃烧,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重13.2g.通过计算,求
某有机物X相对氢气的密度为30,9g该有机物在空气中充分燃烧,燃烧产物依次通过右图所示的装置,实验结束后,称得甲装置增重5.4g,乙装置增重13.2g.通过计算,求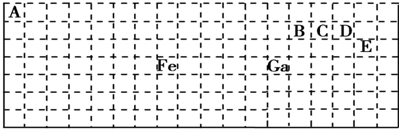
 .
.
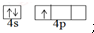
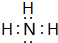 ,含有共价键化学键,E的电子表达式是
,含有共价键化学键,E的电子表达式是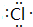 .
.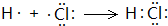 .
.