��Ŀ����
9����2L�������ʵ�����Ϊ0.1mol��Ca2+��Mg2+��ij��Һ�У�����һ������NaOH����ʹ��Һ��pH=ll���г������ɣ����ˣ���֪��KSP[Ca��OH��2]=4.68��10-6��KSP[Mg��OH��2]=5.61��10-12��������Ũ��С��10-5mol•L-1��Ϊ�Ѿ�����������˵����ȷ���ǣ�������| A�� | �˳�����Mg��OH��2��Ca��OH��2�Ļ���� | |
| B�� | �˳���ֻ��Mg��OH��2 | |
| C�� | ���˺���Һ�д���Ca2+��Mg2+ | |
| D�� | ��ԭ��Һ�м���8.8 g NaOH���壬������ʹCa2+����ת��Ϊ���� |
���� ����NaOH�������pH=11����ʱ��Һ��c��OH-��=1��10-3mol•L-1���ɽ��KSP[Ca��OH��2]=4.68��10-6��KSP[Mg��OH��2]=5.61��10-12�����Ƿ��г����������Դ˽����⣮
��� �⣺����NaOH�������pH=11����ʱ��Һ��c��OH-��=1��10-3mol•L-1��
A��Qc[Ca����OH��2]=c��Ca2+������10-3��2=0.05����10-3��2=5��10-8��KSP[Ca��0H��2]����Ca��OH��2���ɣ���A����
B��Q[Mg��OH��2=C��Mg2+������ 10-3��2=0.05����10-3��2=5��10-8��KSP[Mg��OH��2]����Mg��OH��2�������ɣ���B��ȷ��
C������Һ������KSP[Mg��OH��2]=C��Mg2+������10-3��2=5.6��10-12��c��Mg2+��=5.6��10-6��10-5����ʣ�࣬��Һ�в�����Mg2+����C����
D������Ϊ����8.8 g NaOH���壬����n��NaOH��=0.22 mol����0.1 mol Mg2+��Ӧ����OH-0.2 mol��ʣ��0.02 mol OH-������Q[Ca ��OH��2]=c��Ca2+������OH-��2=0.05����0.01��2=5��10-6��KSP[Ca��OH��2]��������Ca��OH��2������������D����
��ѡB��
���� ���⿼�����ܵ���ʵ��ܽ�ƽ���Լ�ת����֪ʶ��Ϊ��Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬��Ŀ�Ѷ��еȣ�ע������ܶȻ��������㲢�����жϣ�������ע����������˼·��

 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д�| A�� | 10 mL 0.1 mol/L AlCl3��Һ | B�� | 20 mL 0.1 mol/L CaCl2��Һ | ||
| C�� | 30 mL 0.2 mol/L KCl��Һ | D�� | 200 mL 2 mol•L-1KClO3��Һ |
| A�� | ��һ���¶���AgClˮ��Һ�У�Ag+��Cl-Ũ�ȵij˻���һ������ | |
| B�� | AgCl��Ksp=1.8��10-10 mol2•L-2�����κκ�AgCl�������Һ�У�c��Ag+��=c��Cl-����Ag+��Cl-Ũ�ȵij˻�����1.8��10-10 mol2•L-2 | |
| C�� | �¶�һ��ʱ������Һ��Ag+��Cl-Ũ�ȵij˻�����Kspֵʱ������ҺΪAgCl�ı�����Һ | |
| D�� | ��2.0mLŨ�Ⱦ�Ϊ0.1mol•L-1��KCl��KI�����Һ�еμ�1��2��0.01mol•L-1 AgNO3��Һ���������ʻ�ɫ��˵��AgCl��Ksp��AgI��KspС |
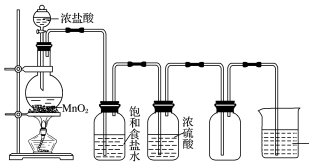
 �����������һ����Ҫ�Ĺ�ҵԭ�ϣ�ij��ѧС�������ͼװ���Ա����ᡢ�״�Ϊԭ����ȡ������������й����ʵ��������ʼ��±���ʾ��
�����������һ����Ҫ�Ĺ�ҵԭ�ϣ�ij��ѧС�������ͼװ���Ա����ᡢ�״�Ϊԭ����ȡ������������й����ʵ��������ʼ��±���ʾ��| ������ | �״� | ��������� | |
| �۵�/�� | 122.4 | -97 | -12.3 |
| �е�/�� | 249 | 64.3 | 199.6 |
| �ܶ�/g��cm-3 | 1.2659 | 0.792 | 1.0888 |
| ˮ���� | �� | ���� | ���� |
��Բ����ƿ�м���0.1mol�������0.4mol �״�����С�ļ��� 3mLŨ���ᣬ���Ⱥ�Ͷ�뼸����ʯ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ��
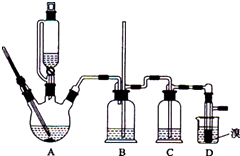
��1����װ�õ������ǣ�������������ȴˮ��b���a����b�����ڽ��룮
��2����ѧС����ʵ�����ù����ķ�Ӧ��״����������Ǹúϳɷ�Ӧ�ǿ��淴Ӧ���״��ȱ�����������Ҽ״��е�ͣ�����ʧ�����Ӽ״�Ͷ������߲��ʣ���߱������ת���ʣ�
�ֲ�Ʒ�ľ���
����������ֲ�Ʒ���������������״������ᡢ�������ˮ�ȣ��������������̽��о���

��1���Լ�1������B�����ţ���������ϴȥ����������й������ᣮ
A��ϡ���� B��̼������Һ C���Ҵ�
��2������2�У��ռ���Ʒʱ�����Ƶ��¶�Ӧ��199.6�����ң�
��3��ʵ���Ƶõı����������Ʒ����Ϊ10g�������ת����Ϊ73.5%�����������λ��Ч���֣���
��4����ʵ���Ƶõı���������IJ����������۲��������ܵ�ԭ����C�����ţ���
A������ʱ��100�濪ʼ�ռ���Ʒ
B���״���������
C���Ʊ���Ʒʱ�����ᱻ������
 ���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶����ߣ�����������ɫ���
���ݻ�Ϊ1.00L�������У�ͨ��һ������N2O4��������ӦN2O4��g��?2NO2��g�������¶����ߣ�����������ɫ���
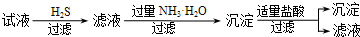
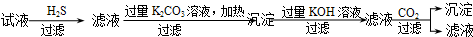

 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�