题目内容
18.下列说法不正确的是( )| A. | 核素23Na的中子数是12 | |
| B. | 16O和18O互为同位素 | |
| C. | 电离方程式:CH3COOH?CH3COOˉ+H+ | |
| D. | 16O、1H、2H、3H四种核素可构成4种水分子 |
分析 A.钠元素质子数为11,质子数+中子数=质量数;
B.质子数相同中子数不同的同种元素的不同原子为同位素;
C.醋酸为弱电解质存在电离平衡;
D.16O、1H、2H、3H四种核素中每两个氢原子和一个氧原子形成水分子.
解答 解:A.钠元素质子数为11,核素23Na的中子数=23-11=12,故A正确;
B.16O和18O质子数相同中子数不同的氧元素的不同原子互为同位素,故B正确;
C.醋酸为弱电解质存在电离平衡,电离方程式:CH3COOH?CH3COOˉ+H+,故C正确;
D.16O、1H、2H、3H四种核素中每两个氢原子和一个氧原子形成水分子,可以正常组成6种水分子,1H2O、2H2O、3H2O、1H2HO、1H3HO、2H3HO,故D错误;
故选D.
点评 本题考查了原子结构、同位素、弱电解质等知识点,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
8.某同学进行下列实验:
下列说法不合理的是( )
| 操作 | 现象 |
 取一块打磨过的生铁片,在其表面滴1滴含酚酞和K3[Fe(CN)6]的食盐水 | 放置一段时间后,生铁片上出现如图所示“斑痕”.其边缘处为红色,中心区域为蓝色,在两色环交界处出现铁锈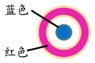 |
| A. | 生铁片发生吸氧腐蚀 | |
| B. | 中心区:Fe-2e-═Fe2+ | |
| C. | 边缘处:O2+2H2O+4e-═4OH- | |
| D. | 交界处:4Fe2++O2+10H2O═4 Fe(OH)3+8H+ |
9.下列鉴别物质或离子的方法能达到目的是( )
| A. | 用氨水鉴别MgCl2溶液和AlCl3溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 用AgNO3鉴别Na2CO3溶液和NaCl溶液 | |
| D. | 用足量的盐酸和BaCl2溶液鉴别溶液中是否含SO42- |
6.某同学对无水乙醇与金属钠的反应进行实验探究.请回答:
(1)仪器a的名称是干燥管.
(2)请写出无水乙醇与钠反应的化学方程式:2CH3CH2OH+2Na=2CH3CH2ONa+H2.
(3)下列有关该实验的说法中,正确的是CD.
A.无水乙醇与钠的反应是吸热反应
B.酸性重铬酸钾溶液的作用是除去乙醇蒸气中混有的氢气
C.仪器a的球形区域对产生的气体起到一定的富集作用,使得气体燃烧的火焰明亮,现象明显
D.操作步骤②中的现象有:加入无水乙醇后,钠表面有气泡,钠开始时沉在液体的底部,然后浮在液面上,直至消失.
| 实验装置 | 操作步骤 | 实验现象 |
 | ①用橡胶管将尖嘴管和仪器a连接,向仪器a的球形区域塞入一团脱脂棉,再向脱脂棉中滴入适量的酸性K2Cr2O7溶液 | 棉花呈橙黄色 |
| ②取黄豆大小的金属钠,用滤纸吸干其表面的煤油,放入小烧杯中,用仪器a的柱体部分扣住金属钠,再向小烧杯中倒入10mL左右无水乙醇,至高度没过金属钠 | ||
| ③反应开始20s左右,点燃尖嘴管处的气体,并在尖嘴管上方罩上内壁涂有澄清石灰水的小烧杯 | 产生明亮的淡蓝色火焰,仪器a内的脱脂棉逐渐由橙黄色变为绿色(Cr3+颜色),烧杯内壁未变浑浊 | |
| ④实验结束后测量反应液的温度 | 反应液的温度为52℃ |
(2)请写出无水乙醇与钠反应的化学方程式:2CH3CH2OH+2Na=2CH3CH2ONa+H2.
(3)下列有关该实验的说法中,正确的是CD.
A.无水乙醇与钠的反应是吸热反应
B.酸性重铬酸钾溶液的作用是除去乙醇蒸气中混有的氢气
C.仪器a的球形区域对产生的气体起到一定的富集作用,使得气体燃烧的火焰明亮,现象明显
D.操作步骤②中的现象有:加入无水乙醇后,钠表面有气泡,钠开始时沉在液体的底部,然后浮在液面上,直至消失.
13.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 1.7 g氨气所含分子数为0.1 NA | |
| B. | 常温常压下,11.2 L氯气所含原子数为NA | |
| C. | 1 mol•L-1的BaCl2溶液中所含Cl-离子数目为2 NA | |
| D. | 71 g氯气与足量铁粉充分反应,转移的电子数为3 NA |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 mL水中含有的分子数目约为1.24NA | |
| B. | 1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等 | |
| C. | 23g钠在氧气中完全燃烧失去电子数为0.5NA | |
| D. | 常温常压下的33.6L氯气与56g铁充分反应,转移电子数为3NA |
10.下列能使品红溶液褪色的是( )
| A. | CO2 | B. | Na2SO3 | C. | Cl2 | D. | HCl |
7.下述实验能达到预期目的是( )
| 编号 | 实验操作 | 实验目的 |
| A | 将甲烷和乙烯的混合气体通过盛有溴水的洗气瓶 | 除去甲烷中混有的乙烯 |
| B | 在苯和苯酚的混合液中加入足量的浓溴水,振荡、过滤 | 分离出苯酚 |
| C | 向CH2=CHCHO溶液中滴入KMnO4酸性溶液 | 证明CH2=CHCHO中含有碳碳双键 |
| D | 先加NaOH溶液共热,然后加入AgNO3溶液 | 检验溴乙烷中含有溴元素 |
| A. | A | B. | B | C. | C | D. | D |
16.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 一定条件下,6.4 g铜与过量的硫反应,转移电子数目为0.2NA | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| C. | 标准状况下,11.2L 水蒸气中含有3NA个原子 | |
| D. | 用石灰乳完全吸收1 mol Cl2时,转移电子的数目是NA |