题目内容
5.设NA表示阿伏伽德罗常数的数值,下列说法错误的是( )| A. | 常温常压下,1 mol氦气含有的核外电子数为2NA | |
| B. | 1.7gCH5+离子中含有的电子总数为NA | |
| C. | lmolC10H22分子中共价键总数为31 NA | |
| D. | lmolNO2与足量水反应时共转移2NA个电子 |
分析 A.氦气为单原子分子;
B.1个CH5+含有10个电子;
C.l个C10H22分子含有22个C-H,9个C-C键;
D.二氧化氮与水反应为歧化反应,求出二氧化氮的物质的量,然后根据3mol二氧化氮转移2mol电子来分析;
解答 解:A.常温常压下,1 mol氦气含有的核外电子数为1mol×1×2×NA=2NA,故A正确;
B.1.7gCH5+离子中含有的电子总数为$\frac{1.7g}{17g/mol}$×10×NA=NA,故B正确;
C.l个C10H22分子含有22个C-H,9个C-C键,则lmolC10H22分子中共价键总数为31 NA,故C正确;
D.二氧化氮与水反应为歧化反应,3mol二氧化氮转移2mol电子,则lmolNO2与足量水反应时共转移$\frac{2}{3}$mol电子,个数为:$\frac{2}{3}$NA,故D错误;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意二氧化氮与水反应为歧化反应特点,注意有机物结构组成,难度不大.

练习册系列答案
相关题目
8.如图为生锈了的家用铁锅,下列有关解释事实的方程式不正确的是( )


| A. | 铁锅生锈过程中有原电池反应,负极反应式是:Fe-2e-=Fe2+ | |
| B. | 铁锅生锈过程中有Fe(OH)3生成:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 用醋可除去铁锈:6CH3COOH+Fe2O3═6CH3COO-+2Fe3++3H2O |
16.下列两组热化学方程式中,有关△H的比较正确的是( )
①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H2
②NaOH(aq)+$\frac{1}{2}$H2SO4(浓)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H3
NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H4.
①CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H2
②NaOH(aq)+$\frac{1}{2}$H2SO4(浓)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H3
NaOH(aq)+CH3COOH(aq)═CH3COONa(aq)+H2O(l)△H4.
| A. | △H1>△H2;△H3<△H4 | B. | △H1>△H2;△H3>△H4 | C. | △H1=△H2;△H3<△H4 | D. | △H1<△H2;△H3>△H4 |
13.仪器名称为“分液漏斗”的是( )
| A. |  | B. |  | C. |  | D. |  |
20.在下列各溶液中,离子不能大量共存的是( )
| A. | 中性溶液中:K+、Fe3+、Cl-、 | |
| B. | Al3+、Cl-、Na+可以大量共存于pH=2的溶液中 | |
| C. | 0.1 mol/L NaAlO2溶液:、Na+、Cl- | |
| D. | 室温下,pH=1的溶液中:Na+、Fe3+ |
10.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | C2H4和C3H6的混合物的质量为a g,所含碳氢键数目为aNA/7 | |
| B. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| D. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为9NA |
17.如图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是.( )
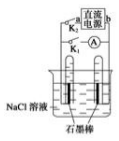

| A. | 若关闭 K2、打开 K1,一段时间后,发现左侧试管收集到的气体比右侧略多 则 a 为正极,b 为负极 | |
| B. | 关闭 K2,打开 K1,一段时间后,用拇指堵住试管移出烧 杯,向试管内滴 入酚酞,发现左侧试管内溶液变红色,则 a 为负极,b 为正极 | |
| C. | 若直流电源 a 为负极,b 为正极,关闭 K2 ,打开 K1,一段时间后,再关闭 K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒 | |
| D. | 若直流电源 a 为负极,b 为正极,关闭 K2,打开 K1,一段时间后,再关闭 K1,打开 K2,则左 侧石墨棒上发生的电极反应为 H2-2e-+2OH-═2H2O |
14.设NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 常温常压下,22.4LH2O中含有分子数为NA | |
| B. | 常温常压下,28gCO和N2的混合物所含的质子数为14NA | |
| C. | 1molCl2分别与足量的铁或氢氧化钠溶液反应,转移电子数均为2NA | |
| D. | 常温下,1mol/L Na2CO3溶液中阴离子总数等于NA |
15.下列装置所示的实验中,能达到目的是( )
| A. |  长时间看到Fe(OH)2白色沉淀 | B. | 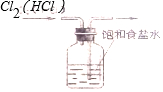 除去Cl2中的HCl杂质 | ||
| C. | 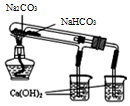 比较NaHCO3、Na2CO3的热稳定性 | D. | 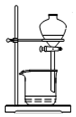 分离碘酒中的碘和酒精 |