题目内容
10.R、W、X、Y、Z为原子序数依次递增的11~18号元素中的五种元素,下列说法一定正确的是(m、n均为正整数)( )| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若HnXOm为强酸,则Y是活泼的非金属元素 | |
| C. | 若Y的最低化合价是-2,则Z的最高正价为+6 | |
| D. | 若X的最高正价为+5,则五种元素都是非金属元素 |
分析 同周期元素的原子,从左到右,元素的金属性从强到弱,最高价氧化物对应的水化物碱性越来越弱,最高正价从+1升到+7价,最高正价等于最外层电子数,以此解答.
解答 解:A.同周期元素从左到右元素的金属性逐渐减弱,若R(OH)n为强碱,则W(OH)m不一定为强碱,故A错误;
B.HnXOm为强酸,则X为N或S,同周期元素从左到右元素非金属性逐渐增强,Y是活泼非金属元素,故B正确;
C.若Y的最低化合价为-2,则Y处于ⅦA族,Z的最低价为-1价,其最高正化合价为+7(F元素除外),故C错误;
D.X的最高正化合价为+5,当X为P,则R一定为金属元素,故D错误.
故选B.
点评 本题考查同周期元素的性质的递变规律,注意把握同周期元素的性质的递变规律和在元素周期表中的可能位置,题目难度不大.

练习册系列答案
相关题目
13.在用锌片、铜片和稀硫酸组成的原电池装置中,经过一段时间后,下列说法正确的是( )
| A. | 铜片上有气泡产生,发生还原反应 | B. | 锌是负极,发生还原反应 | ||
| C. | 电流方向是从锌片沿导线流向铜片 | D. | 铜片逐渐溶解,被氧化 |
1.在一定的温度下,在固定容积的密闭容器中,能表示反应X(气)+2Y(气)?2Z(气)一定达到化学平衡状态的是( )
①容器内压强不随时间改变; ②C(x)•C2(Y)=C2(z);③生成Z的速率与生成Y的速率相等; ④容器内混合气体的密度不随时间改变;⑤X、Y、Z的物质的量之比 1:2:2.
①容器内压强不随时间改变; ②C(x)•C2(Y)=C2(z);③生成Z的速率与生成Y的速率相等; ④容器内混合气体的密度不随时间改变;⑤X、Y、Z的物质的量之比 1:2:2.
| A. | ①③⑤ | B. | ①③ | C. | ②④ | D. | 全部 |
5.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| A. | 己烷(己烯) 溴水 分液 | B. | 淀粉溶液(NaCl) 水 过滤 | ||
| C. | CH3CH2OH(CH3COOH) CaO 蒸馏 | D. | CO2(SO2) Na2CO3溶液 洗气 |
2.某气态烃0.5mol能和1mol HCl充分加成,加成产物1mol又能和6mol Cl2完全取代,则该烃是( )
| A. | C2H6 | B. | C2H2 | C. | C3H4 | D. | C4H6 |
19.下列有机物结构的表示方法不正确的是( )
| A. | 异戊烷的球棍模型: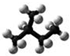 | B. | 乙醇的比例模型: | ||
| C. | 丙烯的结构简式:CH3CHCH2 | D. | 四氯化碳的电子式: |
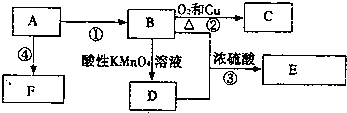

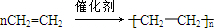 ,反应类型加聚反应.
,反应类型加聚反应.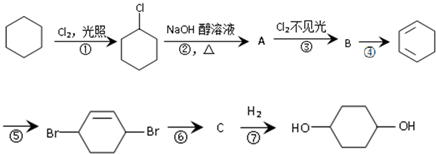
 ;
;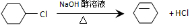
 .
.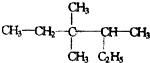 3,3,4-三甲基己烷
3,3,4-三甲基己烷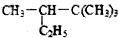 2,2,3-三甲基戊烷
2,2,3-三甲基戊烷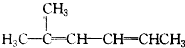 2-甲基-2,4-己二烯
2-甲基-2,4-己二烯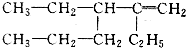 2,3-二乙基-1-己烯.
2,3-二乙基-1-己烯.