题目内容
13.在用锌片、铜片和稀硫酸组成的原电池装置中,经过一段时间后,下列说法正确的是( )| A. | 铜片上有气泡产生,发生还原反应 | B. | 锌是负极,发生还原反应 | ||
| C. | 电流方向是从锌片沿导线流向铜片 | D. | 铜片逐渐溶解,被氧化 |
分析 锌、铜和稀硫酸组成的原电池中,锌作负极,负极上锌失电子发生氧化反应;铜作正极,正极上氢离子得电子发生还原反应;电流从正极流向负极.
解答 解:A.锌、铜和稀硫酸组成的原电池中,铜作正极,正极上氢离子得电子生成氢气,即铜片上会产生大量的气泡,故A正确;
B.锌作负极,负极上锌失电子发生氧化反应,不活泼的金属Cu作正极,故B错误;
C.电流从正极流向负极,即电流由Cu经导线流向Zn,故C错误;
D.铜作正极,正极上氢离子得电子被还原生成氢气,铜片不会溶解,故D错误;
故选A.
点评 本题考查原电池原理,明确正负极上得失电子是解本题关键,难度不大,注意对基础知识的归纳整理.

练习册系列答案
相关题目
3.25℃时,下列无色溶液中由水电离产生的H+是1×10-5mol/L的且能大量共存的是( )
| A. | K+、Na+、NO3-、SO42- | B. | Mg2+、K+、NO3-、Cl- | ||
| C. | Na+、Fe2+、NO3-、Cl- | D. | Ba2+、H+、Cl-、SO42- |
4.根据表中短周期元素性质的数据判断,下列说法一定错误的是( )
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ |
| 原子半径/nm | 0.037 | 0.110 | 0.077 | 0.099 | 0.186 |
| 部分化合价 | +1 | -3+5 | -4+4 | -1 | +1 |
| A. | ④是周期表中非金属性最强的元素 | |
| B. | ①是周期表中原子半径最小的元素 | |
| C. | ②④⑤在位于同一个周期 | |
| D. | ①③两元素组成的最简单化合物分子与③④两元素组成的化合物分子空间构型相同 |
18.在标准状况下,与11.2LN2的分子数目相同CO的物质的量是( )
| A. | 0.2 mol | B. | 0.5mol | C. | 1mol | D. | 2mol |
5.某可充电的锂离子电池以LiMn2O4为正极,嵌入锂的碳材料为负极,含Li+导电固体为电解质.充放电时的电池反应为:Li+LiMn2O4$?_{充电}^{放电}$Li2Mn2O4.下列说法正确的是( )
| A. | 放电时,LiMn2O4发生氧化反应 | |
| B. | 放电时,正极反应为:Li++LiMn2O4+e-═Li2Mn2O4 | |
| C. | 充电时,LiMn2O4发生氧化反应 | |
| D. | 充电时,阳极反应为:Li++e-═Li |
2.有机物C4H9Cl有多少种同分异构体( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
10.R、W、X、Y、Z为原子序数依次递增的11~18号元素中的五种元素,下列说法一定正确的是(m、n均为正整数)( )
| A. | 若R(OH)n为强碱,则W(OH)m也为强碱 | |
| B. | 若HnXOm为强酸,则Y是活泼的非金属元素 | |
| C. | 若Y的最低化合价是-2,则Z的最高正价为+6 | |
| D. | 若X的最高正价为+5,则五种元素都是非金属元素 |
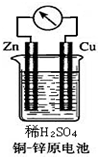 如图所示的铜-锌原电池中,
如图所示的铜-锌原电池中,