题目内容
10.化学是一门以实验为基础的自然科学.某同学需要配制0.1mol•L-1 的NaHCO3溶液500mL,请根据溶液配制过程中的情况回答下列问题:
(1)NaHCO3的俗称小苏打;配制0.1mol•L-1 的NaHCO3溶液时,应称取固体NaHCO3的质量为4.2g.
(2)实验中除了托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒外还需要的其它仪器有500mL容量瓶、胶头滴管;其中两次用到玻璃棒,其作用分别是搅拌、引流.
(3)定容观察液面时俯视刻度线,所配溶液浓度偏高(填“偏高”、“偏低”或“无影响”)
分析 (1)碳酸氢钠俗称小苏打,依据m=CVM计算需要溶质的质量;
(2)依据配制溶液的一般步骤选项需要仪器,依据溶解、移液操作中玻璃棒作用解答;
(3)定容观察液面时俯视刻度线,导致溶液体积偏小,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)碳酸氢钠俗称小苏打,配制0.1mol•L-1 的NaHCO3溶液500mL时,应称取固体NaHCO3的质量m=CVM=0.1mol/L×84g/mol×0.5L=4.2g;
故答案为:小苏打;4.2g;
(2)配制一定物质的量浓度溶液的一般步骤为:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶,用到的仪器:托盘天平(带砝码和镊子)、烧杯、药匙、玻璃棒、500mL容量瓶、胶头滴管,所以还需要的其它仪器有:500mL容量瓶、胶头滴管;
溶解固体时为加速固体溶解速度,用玻璃棒搅拌;引流时为防止液体洒出来,应用玻璃棒将溶液引流入容量瓶;
故答案为:500mL容量瓶、胶头滴管 搅拌、引流;
(3)定容观察液面时俯视刻度线,导致溶液体积偏小,依据C=$\frac{n}{V}$可知溶液浓度偏高;
故答案为:偏高.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,题目难度不大,注意玻璃棒作用及误差分析的方法和技巧.

练习册系列答案
相关题目
6.下列物质不能通过化合反应得到的是( )
| A. | H2SiO3 | B. | FeCl3 | C. | NaHCO3 | D. | Fe3O4 |
18.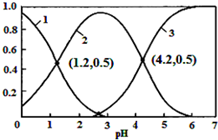 已知H2SO3?HSO3-+H+,Ka1;HSO3-?SO32-+H+,Ka2.常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
已知H2SO3?HSO3-+H+,Ka1;HSO3-?SO32-+H+,Ka2.常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
 已知H2SO3?HSO3-+H+,Ka1;HSO3-?SO32-+H+,Ka2.常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )
已知H2SO3?HSO3-+H+,Ka1;HSO3-?SO32-+H+,Ka2.常温下,向某浓度的H2SO3溶液中逐滴加入一定量浓度的NaOH溶液,所得溶液中H2SO3、HSO3-、SO32-三种微粒的物质的量分数(δ)与溶液pH的关系如图所示,则下列说法中不正确的是( )| A. | pH=1.2溶液中:c(Na+)+c(H+)═c(OH-)+c(H2SO3) | |
| B. | 常温下,$\frac{{c}^{2}(HS{{O}_{3}}^{-})}{c({H}_{2}S{O}_{3})•c(S{{O}_{3}}^{2-})}$=1000 | |
| C. | 向pH=1.2的溶液中加KOH溶液将pH增大至4.2的过程中水的电离度先增大后减小 | |
| D. | 曲线3表示的微粒是SO32- |
2.化学与生产、生活、环境密切相关,下列说法中正确的是( )
| A. | 食盐、次氯酸钠溶液均可以将某些病毒氧化而达到消毒的目的 | |
| B. | 大力实施矿物燃料“脱硫、脱硝”技术,可减少酸雨的发生 | |
| C. | 光纤通信使用的光缆的主要成分是晶体Si,太阳能电池使用的材枓主要是SiO2 | |
| D. | 节日燃放的烟花,是碱金属、锶、铂、铁等金属化合物焰色反应所呈现的色彩 |
20.反应Cl2+2KI═2KCl+I2中,氧化剂是( )
| A. | Cl2 | B. | KI | C. | KCl | D. | I2 |

 ;YW2分子形状为直线形.
;YW2分子形状为直线形.