题目内容
用石墨电极电解500mLNaNO3和Cu(NO3)2的混合溶液.通电一段时间后,阴、阳两极逸出的气体在标准状况下的体积分别为11.2L和8.4L,求原溶液中Cu2+的物质的量浓度(假设溶液的体积不变)( )
| A、1.25 mol?L-1 |
| B、2.5 mol?L-1 |
| C、0.50 mol?L-1 |
| D、1.0 mol?L-1 |
考点:电解原理
专题:电化学专题
分析:阳极溶液中离子放电顺序书写电极反应,溶液中阴离子氢氧根离子失电子生成氧气,阳离子放电顺序Cu2+>H+,阳极电极反应为:4OH--4e-=2H2O+O2↑,阴极电极反应为:Cu2++2e-=Cu 2H++2e-=H2↑,依据两极生成气体物质的量结合电解过程中电子守恒计算得到.
解答:
解:阳极溶液中离子放电顺序书写电极反应,溶液中阴离子氢氧根离子失电子生成氧气,阳离子放电顺序Cu2+>H+,阳极电极反应为:4OH--4e-=2H2O+O2↑,阴极电极反应为:Cu2++2e-=Cu、2H++2e-=H2↑,阴、阳两极逸出的气体在标准状况下的体积分别为11.2L即0.5mol和8.4L即
=0.375mol,依据电子守恒电极主要电子为4×0.375mol=1.5mol,生成氢气转移电子0.5mol×2=1mol,铜离子得到电子1.5mol-1mol=O.5mol,反应的铜离子物质的量0.25mol,所以Cu2+的物质的量浓度=
=0.5mol/L,
故选C.
| 8.4 |
| 22.4 |
| 0.25mol |
| 0.5L |
故选C.
点评:本题考查了电极原理的计算应用,注意电子守恒的计算应用和正确书写电极反应,题目难度中等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述不正确的是( )
| A、常温下,1 mol 铁放入足量的浓硫酸中转移的电子数为0 | ||
B、标准状况下,密度为ρg?L-1的某气体纯净物一个分子的质量为
| ||
| C、将1mol Cl2通入到水中,得到的氯水中,N(HClO)+N(Cl-)+N(ClO-)<2NA | ||
| D、在含有4mol Si-O键的石英晶体中,氧原子的数目为2NA |
25℃时,下列各组离子在指定溶液中一定大量共存的是( )
| A、pH=13的溶液:Cu2+、NH4+、NO3-、SO42- |
| B、含0.1 mol/L Fe3+的溶液:NH4+、Na+、Cl-、SO32- |
| C、滴入甲基橙试剂变红色的溶液:Na+、K+、AlO2-、SO42- |
| D、c(H+)=10-13 mol?L-1的溶液:K+、Na+、CO32-、Br- |
下列反应中,氧化剂与还原剂物质的量的关系为1:2的是( )
| A、O3+2KI+H2O═2KOH+I2+O2 |
| B、2CH3COOH+Ca(CIO)2═2HClO+(CH3COO)2Ca |
| C、I2+2NaClO3═2NalO3+Cl2 |
| D、4HCl(浓)+MnO2═MnCl2+Cl2↑+2H2O |
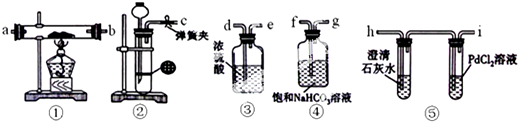
 在实验室中,制得纯净的气体,往往需要对气体进行干燥,某同学用如图所示装置干燥铁粉与水蒸气在高温条件下反应所得的H2,在干燥管中加入CaO固体,干燥后的H2点不燃,通过测定,发现是CaO固体变质导致的.
在实验室中,制得纯净的气体,往往需要对气体进行干燥,某同学用如图所示装置干燥铁粉与水蒸气在高温条件下反应所得的H2,在干燥管中加入CaO固体,干燥后的H2点不燃,通过测定,发现是CaO固体变质导致的. 对叔丁基苯酚
对叔丁基苯酚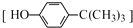 可用于生产油溶性酚醛树脂等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下:
可用于生产油溶性酚醛树脂等.实验室以苯酚、叔丁基氯[(CH3)3CCl]等为原料制备对叔丁基苯酚的实验步骤如下: