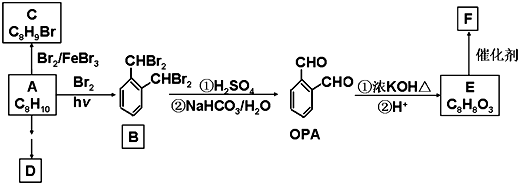
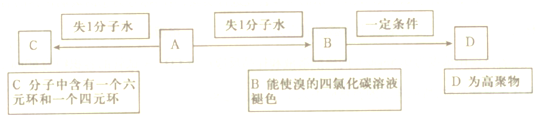
题目内容
短周期元素A、B、C、D、E五种元素的原子序数依次增大,已知A元素形成的单质是密度最小的气体(标准状况下),A和B的原子序数之和等于C的原子序数,B与A、C与A形成的化合物的电子数等于D3+的电子数;而xE-的核外电子排布示意图为 请按要求填空:
请按要求填空:
(1)若C元素形成的单质是最活泼的非金属单质,请写出由A、B两元素构成的具有非极性键的极性分子的电子式: .
(2)若C元素构成的单质是人类呼吸中不能缺少的物质,请写出由A、B、C、D、E五种元素中的一种或几种构成的具体物质做反应物,各写出一个符合下列要求的化学方程式:
①置换反应(含有D元素): .
②非分解反应的氧化还原反应(E元素的价态从中间态到一高一低): .
③由A:B:C=4:2:3构成的物质的溶液中离子浓度大小顺序是: .
④写出电解NaE溶液(足量多)如何用化学方法检验阳极区的产物: .
 请按要求填空:
请按要求填空:(1)若C元素形成的单质是最活泼的非金属单质,请写出由A、B两元素构成的具有非极性键的极性分子的电子式:
(2)若C元素构成的单质是人类呼吸中不能缺少的物质,请写出由A、B、C、D、E五种元素中的一种或几种构成的具体物质做反应物,各写出一个符合下列要求的化学方程式:
①置换反应(含有D元素):
②非分解反应的氧化还原反应(E元素的价态从中间态到一高一低):
③由A:B:C=4:2:3构成的物质的溶液中离子浓度大小顺序是:
④写出电解NaE溶液(足量多)如何用化学方法检验阳极区的产物:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:已知A元素形成的单质是密度最小的气体(标准状况下),应为H元素,xE-的核外电子排布示意图为 ,可知E为Cl元素,x=17,
,可知E为Cl元素,x=17,
B与A、C与A形成的化合物的电子数等于D3+的电子数,D应为Al,离子的电子数为10,
A和B的原子序数之和等于C的原子序数,A的原子序数为1,则B、C相邻,B与A、C与A形成的化合物的电子数等于D3+的电子数,如B为C、则C为N,如B为N,则C为O,如B为O,则C为F,结合题目要求解答该题.
 ,可知E为Cl元素,x=17,
,可知E为Cl元素,x=17,B与A、C与A形成的化合物的电子数等于D3+的电子数,D应为Al,离子的电子数为10,
A和B的原子序数之和等于C的原子序数,A的原子序数为1,则B、C相邻,B与A、C与A形成的化合物的电子数等于D3+的电子数,如B为C、则C为N,如B为N,则C为O,如B为O,则C为F,结合题目要求解答该题.
解答:
解:已知A元素形成的单质是密度最小的气体(标准状况下),应为H元素,xE-的核外电子排布示意图为 ,可知E为Cl元素,x=17,
,可知E为Cl元素,x=17,
B与A、C与A形成的化合物的电子数等于D3+的电子数,D应为Al,离子的电子数为10,
A和B的原子序数之和等于C的原子序数,A的原子序数为1,则B、C相邻,B与A、C与A形成的化合物的电子数等于D3+的电子数,如B为C、则C为N,如B为N,则C为O,如B为O,则C为F,
(1)若C元素形成的单质是最活泼的非金属单质,应为F2,则B为O元素,由A、B两元素构成的具有非极性键的极性分子为H2O2,电子式为 ,
,
故答案为: ;
;
(2)若C元素构成的单质是人类呼吸中不能缺少的物质,应为O元素,则B为N元素,
①D为Al,可与HCl反应生成氢气,化学方程式为2Al+6HCl=2AlCl3+3H2↑,为置换反应,故答案为:2Al+6HCl=2AlCl3+3H2↑;
②E为Cl,元素的价态从中间态到一高一低,可发生歧化反应,如Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO;
③由A:B:C=4:2:3构成的物质为NH4NO3,NH4+水解呈酸性,离子浓度大小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(NO3-)>c(NH4+)>c(H+)>c(OH-);
④电解NaCl溶液,阳极生成氯气,可用湿润的淀粉KI试纸检验,若变蓝,则说明生成了氯气,
故答案为:用湿润的淀粉KI试纸检验,若变蓝,则说明生成了氯气.
 ,可知E为Cl元素,x=17,
,可知E为Cl元素,x=17,B与A、C与A形成的化合物的电子数等于D3+的电子数,D应为Al,离子的电子数为10,
A和B的原子序数之和等于C的原子序数,A的原子序数为1,则B、C相邻,B与A、C与A形成的化合物的电子数等于D3+的电子数,如B为C、则C为N,如B为N,则C为O,如B为O,则C为F,
(1)若C元素形成的单质是最活泼的非金属单质,应为F2,则B为O元素,由A、B两元素构成的具有非极性键的极性分子为H2O2,电子式为
 ,
,故答案为:
 ;
;(2)若C元素构成的单质是人类呼吸中不能缺少的物质,应为O元素,则B为N元素,
①D为Al,可与HCl反应生成氢气,化学方程式为2Al+6HCl=2AlCl3+3H2↑,为置换反应,故答案为:2Al+6HCl=2AlCl3+3H2↑;
②E为Cl,元素的价态从中间态到一高一低,可发生歧化反应,如Cl2+H2O=HCl+HClO,故答案为:Cl2+H2O=HCl+HClO;
③由A:B:C=4:2:3构成的物质为NH4NO3,NH4+水解呈酸性,离子浓度大小顺序为c(NO3-)>c(NH4+)>c(H+)>c(OH-),
故答案为:c(NO3-)>c(NH4+)>c(H+)>c(OH-);
④电解NaCl溶液,阳极生成氯气,可用湿润的淀粉KI试纸检验,若变蓝,则说明生成了氯气,
故答案为:用湿润的淀粉KI试纸检验,若变蓝,则说明生成了氯气.
点评:本题考查了元素位置结构性质的关系及应用,涉及离子浓度大小比较、电解原理、电子式的书写等知识点,根据元素周期表及原子结构确定元素,正确推断元素是解本题关键,题目难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
2008年是不平凡的一年,有悲痛也有激动,下列说法中有关化学的知识正确的是( )
| A、美丽的“水立方”是北京奥运会游泳馆,设计灵感来自于有机细胞的天然图案以及肥皂泡的形成.在这个中心的蓝色泡墙之内,钢结构的基本单位是一个由12个正五边形和2个正六边形组成的几何细胞,覆盖这个框架的是半透明的“气泡”,称为ETFE,该材料为四氟乙烯(CF2=CF2)与乙烯的共聚物,ETFE属于有机物中的烃类. |
| B、5月12日四川汶川发生特大地震,为防止在大灾之后疫病流行,全国各地向灾区运送了大量的各种消毒剂、漂白剂,如:Ca(ClO)2、ClO2、Al(OH)3等. |
| C、美国科学家马丁?查非(Martin Chalfie)、美国华裔化学家钱永健(Roger Tsien)以及日本科学家下村修(Osamu Shimomura)因发现和研究绿色荧光蛋白(green fluorescent protein,GFP)而获2008年度诺贝尔化学奖.向GFP中加入重金属离子,GFP就会变性. |
| D、神舟七号载人飞船于2008年9月25日21点10分发射升空.中国航天员首次空间出舱活动.“神舟七号”的燃料是氢化锂三兄弟--LiH、LiD、LiT.其中Li的质量数为7,这三种物质的化学性质不相同. |
下列实验操作与安全事故处理正确的是( )
| A、金属钠着火时可用干粉灭火器扑灭 |
| B、在硫酸铜晶体结晶水含量测定的实验中,称量操作至少需要四次 |
| C、铜与浓硫酸反应时,用蘸有浓溴水的棉花放在导管口吸收多余的气体 |
| D、在250 mL烧杯中加入216 mL水和24 g NaOH固体,配制10%NaOH溶液 |
下列各种情况下,溶液中可能大量存在的离子组是( )
| A、由水电离出的c(H+)=l×10-12mol/L、的溶液中:K+、Ba2+、OH-、NO3- |
| B、澄清透明的溶液中:I-、Cl-、ClO-、Na+ |
| C、使pH试纸呈红色的溶液中:K+、Fe2+、NO3-、MnO4- |
| D、含有S2O32-的溶液中:K+、Na+、H+、SO42- |
两种气态烃的混合物1L,在空气中完全燃烧生成1.5LCO2气体和2L水蒸气(均在标准状况下测定).关于混合物的说法正确的是( )
| A、一定有甲烷 |
| B、一定有乙烷 |
| C、一定含有甲烷,不一定含有乙烷 |
| D、可能是甲烷和丙烷的混合物 |