题目内容
6.工业生产过程中处处体现化学变化的无穷魅力,请用化学方程式说明下列变化.(1)在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:向废液中投入过量铁屑,充分反应后分离出固体和滤液;向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气.FeCl3蚀刻铜箔反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+,鼓入空气时的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3.
(2)铝土矿(主要成分是Al2O3)在提炼时首先用NaOH溶液溶解,其离子方程式为Al2O3+2OH-=2AlO2-+H2O.
(3)工业上制得 NO的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.氮氧化物(NO和NO2)污染环境,若用Na2CO3溶液吸收NO和NO2(两种气体体积之比1:1),可生成CO2和一种盐.则反应的离子方程式为NO+NO2+CO32-=CO2+2NO2-.
分析 (1)FeCl3蚀刻铜箔反应生成氯化亚铁、氯化铜;鼓入空气时氢氧化亚铁被氧化生成氢氧化铁;
(2)氧化铝与NaOH反应生成偏铝酸钠和水;
(3)氨气催化氧化生成NO;用Na2CO3溶液吸收NO和NO2(两种气体体积之比1:1),可生成CO2和一种盐,由氧化还原反应原理可知生成盐为NaNO2,N元素的化合价为+3价,在+2、+4之间,以此来解答.
解答 解:(1)FeCl3蚀刻铜箔反应生成氯化亚铁、氯化铜,离子反应为2Fe3++Cu=2Fe2++Cu2+;鼓入空气时氢氧化亚铁被氧化生成氢氧化铁,发生的反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:2Fe3++Cu=2Fe2++Cu2+;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)氧化铝与NaOH反应生成偏铝酸钠和水,离子反应为Al2O3+2OH-=2AlO2-+H2O,故答案为:Al2O3+2OH-=2AlO2-+H2O;
(3)氨气催化氧化生成NO,反应为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;用Na2CO3溶液吸收NO和NO2(两种气体体积之比1:1),可生成CO2和一种盐,由氧化还原反应原理可知生成盐为NaNO2,N元素的化合价为+3价,在+2、+4之间,离子反应为NO+NO2+CO32-=CO2+2NO2-,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;NO+NO2+CO32-=CO2+2NO2-.
点评 本题考查物质的性质及离子反应、化学反应的书写,为高频考点,把握习题中的信息、氧化还原反应原理、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案(1)活性炭可用于处理大气污染物NO,在1L恒容密闭容器中加入0.100mol NO和2.030mol固体活性炭(无杂质),生成气体E和气体F.当温度分别在T1℃和T2℃时,测得平衡时各物质的物质的量如下表:
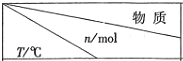 | 活性炭 | NO | E | F |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应的平衡常数表达式K=$\frac{c({N}_{2})c(C{O}_{2})}{{c}^{2}(NO)}$,根据上述信息判断,T1和T2的关系是C;
A.T1>T2B.T1<T2C.无法比较
③在T1℃下反应达到平衡后,下列措施能改变NO的转化率的是cd;
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(2)碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得H2,具体流程如图1所示
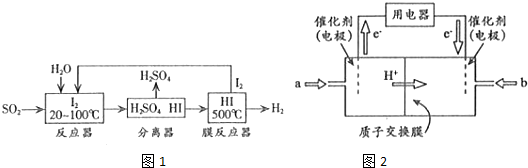
①用离子方程式表示反应器中发生的反应SO2+I2+2H2O=SO42-+2I-+4H+;
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是HI分解为可逆反应,及时分离出产物H2,有利于反应正向进行;
(3)开发新能源是解决大气污染的有效途径之一.直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注.DMFC工作原理如图2所示
通过a气体的电极是原电池的负极(填“正”或“负”),b电极反应式为O2+4e-+4H+=2H2O.
| 元素 | 结构或性质信息 |
| T | 原子的L层上s电子数等于p电子数. |
| X | 元素的原子半径是第三周期主族元素中最大的. |
| Y | 空气中含其单质,原子的最外层未成对电子数是该元素所在周期中最多的. |
| Z | 单质常温、常压下是气体.原子的M层上有1个未成对的p电子. |
(1)写出与Y2互为等电子体的分子式CO;
(2)T、X、Y三种元素的电负性由大到小的顺序(填元素符号)是N>C>Na;
(3)元素Q的原子序数是X与Z的原子序数之和.
①该元素基态原子的外围电子排布式为3d84s2;
②元素Q与元素T、Y、Z分别形成平面型的[Q(TY)4]2-和四面体的[QZ4]2-,Q的配位数为4,其中T与Y、Q与Z成键时中心原子采用的杂化方式分别是sp、sp3.
 有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入Na2O2,得到的沉淀量与加入的Na2O2的关系如图所示,则原溶液中MgCl2、Al2(SO4)3的物质的量浓度之比为( )
有MgCl2、Al2(SO4)3的混合溶液,向其中不断加入Na2O2,得到的沉淀量与加入的Na2O2的关系如图所示,则原溶液中MgCl2、Al2(SO4)3的物质的量浓度之比为( )| A. | 1:2 | B. | 2:3 | C. | 6:1 | D. | 2:1 |
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | L与Q形成的化合物化学式为LQ | |
| B. | L、M的单质与稀盐酸反应剧烈程度:M>L | |
| C. | Q、T的氢化物在常温常压下均为无色气体 | |
| D. | M的最高价氧化物的水化物不具有两性 |
| A. | 砷的第一电离能高于磷而电负性低于磷 | |
| B. | 三氯化砷与三氯化氮分子都是三角锥构型 | |
| C. | 最高氧化物对应水化物的化学式为HAsO3 | |
| D. | 砷的第一电离能小于同周期硒的电离能 |
| A. | 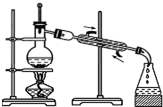 分离沸点相差较大液体混合物 | B. | 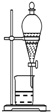 分离互不相溶的两种液体 | ||
| C. | 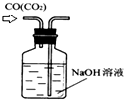 除去CO气体中的CO2气体 | D. | 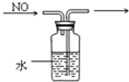 排水集气法收集NO |