题目内容
某无色溶液中粒子能大量共存,通入CO2后仍能大量共存的一组是( )
| A、K+、SO42-、Br-、SiO32- |
| B、H+、Fe2+、Cl-、NH4+ |
| C、Na+、Ba2+、NO3-、Cl- |
| D、Na+、Ag+、NH3?H2O、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:无色溶液中不存在 Cu2+、Fe2+、Fe3+、MnO4-等有色离子,
A.硅酸根离子与二氧化碳反应生成硅酸沉淀;
B.亚铁离子为有色离子,不满足溶液无色的要求;
C.Na+、Ba2+、NO3-、Cl-离子之间不反应,都是无色离子,通入二氧化碳后也不反应;
D.银离子与氨水发生反应,氨水与二氧化碳反应.
A.硅酸根离子与二氧化碳反应生成硅酸沉淀;
B.亚铁离子为有色离子,不满足溶液无色的要求;
C.Na+、Ba2+、NO3-、Cl-离子之间不反应,都是无色离子,通入二氧化碳后也不反应;
D.银离子与氨水发生反应,氨水与二氧化碳反应.
解答:
解:A.在溶液中SiO32-与CO2发生反应生成硅酸,在溶液中不能大量共存,故A错误;
B.Fe2+为有色离子,不满足溶液无色的条件,故B错误;
C.Na+、Ba2+、NO3-、Cl-之间不发生反应,通入二氧化碳后仍然不反应,且为无色溶液,在溶液中能够大量共存,故C正确;
D.Ag+、NH3?H2O之间反应,二氧化碳与NH3?H2O反应,在溶液中不能大量共存,故D错误;
故选C.
B.Fe2+为有色离子,不满足溶液无色的条件,故B错误;
C.Na+、Ba2+、NO3-、Cl-之间不发生反应,通入二氧化碳后仍然不反应,且为无色溶液,在溶液中能够大量共存,故C正确;
D.Ag+、NH3?H2O之间反应,二氧化碳与NH3?H2O反应,在溶液中不能大量共存,故D错误;
故选C.
点评:本题考查离子共存的正误判断,是高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
标准状况下电解200mLNaCl、CuSO4的混合溶液,阴阳两极所得气体的体积随时间变化如图所示,则c(CuSO4)为( )
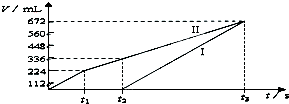

| A、0.1mol/L |
| B、0.15mol/L |
| C、0.2mol/L |
| D、0.25mol/L |
已知反应:①Cl2+2KBr=2KCl+Br2;②KClO3+6HCl=3Cl2↑+KCl+3H2O;③2KBrO3+Cl2=Br2+2KClO3下列说法错误的是( )
| A、氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 |
| B、①中KCl是氧化产物,KBr 发生还原反应 |
| C、③中2mol氧化剂参加反应得到电子的物质的量为10 mol |
| D、反应②中氧化剂与还原剂的物质的量之比为1:6 |
下列说法中不正确的是( )
| A、大型中央空调的制冷剂可用液氨 |
| B、工业上用H2和N2合成氨与自然界中放电时O2和N2反应都属于氮的固定 |
| C、常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
| D、铵盐易溶于水,且可与强碱发生复分解反应 |
实验室需配制一种仅含四种离子(不包括水电离出的离子)的混合溶液,且在混合液中四种离子的物质的量浓度均为0.5mol/L,下面四个选项中能达到此目的是( )
| A、Fe2+、Na+、NO3-、Cl- |
| B、Mg2+、NH4+、SO42-、NO3- |
| C、H+、K+、Cl-、CH3COO- |
| D、Fe3+、K+、AlO2-、SO42- |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C、某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、标准状态下,33.6L氟化氢中含有氟原子的数目为1.5NA |
下列离子方程式表达正确的是( )
| A、0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O |
| B、氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+ |
| C、Ca(HCO3)2溶液中滴加过量的NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| D、用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-=2AlO2-+H2O |