题目内容
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,7.0g乙烯与丙烯的混合物中含有氢原子的数目为NA |
| C、某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目为0.6NA |
| D、标准状态下,33.6L氟化氢中含有氟原子的数目为1.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氯气与水的反应是可逆反应,不能进行彻底;
B、根据乙烯和丙烯的最简式均为CH2来计算;
C、合成氨的反应为可逆反应,不能进行彻底;
D、标况下,HF为液态.
B、根据乙烯和丙烯的最简式均为CH2来计算;
C、合成氨的反应为可逆反应,不能进行彻底;
D、标况下,HF为液态.
解答:
解:A、氯气与水的反应是可逆反应,不能进行彻底,故0.1molCl2溶于水,转移的电子数目小于0.1NA,故A错误;
B、乙烯和丙烯的最简式均为CH2,则7.0g的混合物中CH2的物质的量n=
=
=0.5mol,氢原子的物质的量为1mol,数目为NA,故B正确;
C、合成氨的反应为可逆反应,不能进行彻底,故0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目小于0.6NA,故C错误;
D、标况下,HF为液态,故D错误.
故选B.
B、乙烯和丙烯的最简式均为CH2,则7.0g的混合物中CH2的物质的量n=
| m |
| M |
| 7.0g |
| 14g/mol |
C、合成氨的反应为可逆反应,不能进行彻底,故0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目小于0.6NA,故C错误;
D、标况下,HF为液态,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
根据下列金属的熔沸点其中不能形成合金的是( )
| 金属 | Na | Cu | Al | Fe |
| 熔点(℃) | 97.5 | 1 083 | 660 | 1 535 |
| 沸点(℃) | 883 | 2 595 | 2 200 | 3 000 |
| A、Cu与Al |
| B、Fe与Cu |
| C、Fe与Na |
| D、Al与Na |
下列各溶液中一定能大量共存的离子组是( )
| A、加入铝粉有氢气生成的溶液中:Mg2+、Cu2+、SO42-、K+ |
| B、使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C、常温下,c(H+)=10-14mol/L的溶液中:Na+、AlO2-、S2-、SO32- |
| D、常温下,水电离出的c(H+)与c(OH-)乘积为10-28的溶液中:K+、Na+、HCO3-、Ca2+ |
某无色溶液中粒子能大量共存,通入CO2后仍能大量共存的一组是( )
| A、K+、SO42-、Br-、SiO32- |
| B、H+、Fe2+、Cl-、NH4+ |
| C、Na+、Ba2+、NO3-、Cl- |
| D、Na+、Ag+、NH3?H2O、NO3- |
下列说法不正确的是( )
| A、两个原子之间形成共价键时,最多有一个σ键 |
| B、σ键比π键重叠程度大,形成的共价键强 |
| C、N2分子中有一个σ键,2个π键 |
| D、气体单质中,一定有σ键,可能有π键 |
用铁片与稀硫酸反应制取氢气时,下列措施不能使氢气的生成速率加快的是( )
| A、通入HCl气体 |
| B、不用铁片,改用铁粉 |
| C、滴加少量硫酸铜溶液 |
| D、加入KNO3固体 |
利用焰色反应,人们在烟花中有意识地加入特定金属元素,使焰火更加绚丽多彩.下列说法中正确的是( )
| A、非金属单质燃烧时火焰均为无色 |
| B、NaCl与Na2CO3灼烧时火焰颜色相同 |
| C、焰色反应均应透过蓝色钴玻璃观察 |
| D、只有金属单质灼烧时火焰才有颜色 |
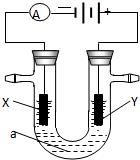 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: