题目内容
某溶液中加入铝粉,有H2放出,在该溶液中一定能大量共存的离子组是( )
| A、K+、Na+、Cl-、SO42- |
| B、Na+、NH4+、SO42-、HCO3- |
| C、Na+、Ba2+、NO3-、Cl- |
| D、K+、Na+、NO3-、AlO2- |
考点:离子共存问题
专题:离子反应专题
分析:加入铝粉,有H2放出,则溶液为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、水、气体等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答:
解:加入铝粉,有H2放出,则溶液为非氧化性酸或强碱溶液,
A.酸、碱溶液中离子之间均不反应,可大量共存,故A选;
B.碱溶液中不能存在NH4+、HCO3-,酸溶液中不能存在HCO3-,故B不选;
C.酸溶液中Al、H+、NO3-发生氧化还原反应,不能生成氢气,故C不选;
D.酸溶液中Al、H+、NO3-发生氧化还原反应,不能生成氢气,故D不选;
故选A.
A.酸、碱溶液中离子之间均不反应,可大量共存,故A选;
B.碱溶液中不能存在NH4+、HCO3-,酸溶液中不能存在HCO3-,故B不选;
C.酸溶液中Al、H+、NO3-发生氧化还原反应,不能生成氢气,故C不选;
D.酸溶液中Al、H+、NO3-发生氧化还原反应,不能生成氢气,故D不选;
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,注意CD中硝酸根离子的氧化性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组溶液中,只用试管和胶头滴管,不用其他任何试剂就能鉴别的是( )
| A、AlCl3和NaOH |
| B、KCl和NaCl |
| C、NaCl和AgNO3 |
| D、Na2CO3和Ba(OH)2 |
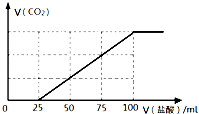 向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )
向100mL NaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是( )| A、原NaOH溶液的浓度为0.2 mol/L |
| B、通入CO2的体积为448 mL |
| C、所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3 |
| D、所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1 |
在1L密闭容器发生反应:4NH3(g)+5O2(g)?4NO(g)+6HO(g)△H=-Q kJ?mol-1(Q>0),容器内部分物质的物质的量浓度如下表:
下列说法错误的是( )
| 时间/浓度 | c(NH3)(mol?L-1) | c(O2)(mol?L-1) | c(NO)(mol?L-1) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.2 |
| 第4min | 0.3 | 0.975 | 0.5 |
| 第6min | 0.3 | 0.975 | 0.5 |
| 第8min | 0.7 | 1.475 | 0.1 |
| 第10min | 0.7 | 1.475 | 0.1 |
| A、反应在第2min到第4min时,O2的平均速率为0.1875mol?L-1?min-1 |
| B、反应在第2min时改变了某一条件,该条件可能是使用催化剂或升高温度 |
| C、第4min、第8min时分别达到化学平衡,且平衡常数相同 |
| D、在开始反应的前2min内,该反应放出0.05QKJ的热量 |
下列说法正确的是( )
A、
| ||||
B、
| ||||
C、Cl-的粒子结构示意图为 | ||||
| D、不同的核素属于不同的元素 |
下列各组分子中,都属于含极性键的非极性分子的是( )
| A、CO2 H2S |
| B、C60 C2H4 |
| C、C2H4 CH4 |
| D、NH3 HCl |