题目内容
对于H2O2分解反应,Cu2+也有一定的催化作用.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
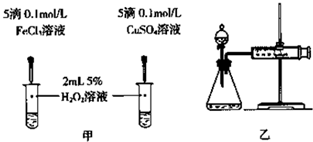
①定性分析:如图甲可通过观察 ,定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是 .
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是 .

①定性分析:如图甲可通过观察
②定量分析:用图乙所示装置做对照实验,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略.实验中需要测量的数据是
考点:探究影响化学反应速率的因素
专题:实验设计题,化学反应速率专题
分析:①根据反应生成气体的快慢分析;根据H2O2分解的催化作用有可能是氯离子起的作用,改为Fe2(SO4)3使阳离子相同,更为合理;
②根据反应速率的表达式v=
进行分析实验中需要测量的数据.
②根据反应速率的表达式v=
| △c |
| △t |
解答:
解:①该反应中产生气体,而且反应放热,所以可根据反应产生气泡快慢来判断反应速率大小,
H2O2分解的催化作用有可能是氯离子起的作用,改为Fe2(SO4)3使阳离子相同,这样可以控制阴离子相同,排除阴离子的干扰,更为合理,
故答案为:反应产生气泡快慢;控制阳离子相同,排除阳离子的干扰;
②根据反应速率v=
可知,实验中需要测量反应的时间,或收集40mL气体所需要的时间,从而判断反应速率快慢,
故答案为:时间(或收集40mL气体所需要的时间).
H2O2分解的催化作用有可能是氯离子起的作用,改为Fe2(SO4)3使阳离子相同,这样可以控制阴离子相同,排除阴离子的干扰,更为合理,
故答案为:反应产生气泡快慢;控制阳离子相同,排除阳离子的干扰;
②根据反应速率v=
| △c |
| △t |
故答案为:时间(或收集40mL气体所需要的时间).
点评:本题考查了催化剂的作用及化学反应速率的影响因素等知识点,题目难度不大,要明确将FeCl3改为Fe2(SO4)3更为合理的理由,试题侧重考查学生的分析、理解能力.

练习册系列答案
相关题目
想一想:NaOH、CuSO4、CH3COOH这些物质为什么可以归为一类,下列哪些物质还可以和它们归为一类( )
| A、CO2 |
| B、HCl(气态) |
| C、Fe(OH)3胶体 |
| D、NaOH溶液 |
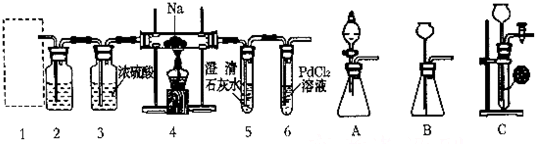
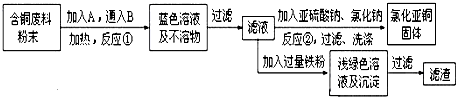
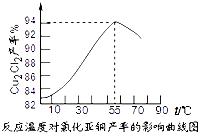 氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知:
氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知: