题目内容
 氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知:
氯化亚铜(Cu2Cl2)是一种重要的化工产品,常用作有机合成催化剂.已知:a.Cu2Cl2不溶于乙醇,在空气中会被迅速氧化;
b.在pH≥4时,Cu2+开始以碱式盐形式沉淀;
c.Cu2Cl2能溶于浓盐酸生成配合物,该配合物加水稀释后会重新析出Cu2Cl2沉淀.
(1)Cu2Cl2的盐酸溶液能吸收CO而生成复合物氯化羰基亚铜[Cu2Cl2(CO)2?2H2O].该反应的化学方程式为
(2)工业上处理、回收含铜电缆废料制备氯化亚铜的方案如下:
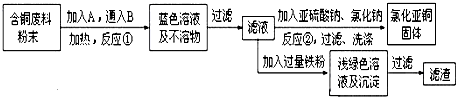
①反应①符合绿色化学思想,则稀酸A为
②反应②的离子方程式是
为提高Cu2Cl2的产率,工业上常在反应②的溶液中加入适量稀碱溶液,控制pH为3.5左右,其目的是
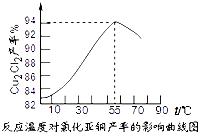
③保持各反应物的最佳配比,改变温度,测得Cu2Cl2产率的变化如图所示,则反应最佳温度为
④析出的氯化亚铜晶体要立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装.真空干燥,密封包装的目的是
考点:制备实验方案的设计,化学平衡建立的过程,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题,化学平衡专题
分析:(1)根据题目信息书写化学方程式;
(2)①金属铜和稀硫酸不反应,但是在鼓入氧气的条件下会发生反应生成硫酸铜;
②根据化学平衡移动原理:减少生成物的浓度,化学平衡正向移动来分析;
③根据此温度下CuCl产率最大;
④根据立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装.真空干燥,密封包装说明氯化亚铜在空气中会被氧化而变质;
(2)①金属铜和稀硫酸不反应,但是在鼓入氧气的条件下会发生反应生成硫酸铜;
②根据化学平衡移动原理:减少生成物的浓度,化学平衡正向移动来分析;
③根据此温度下CuCl产率最大;
④根据立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装.真空干燥,密封包装说明氯化亚铜在空气中会被氧化而变质;
解答:
解:(1)由Cu2Cl2的盐酸溶液能吸收CO而生成复合物氯化羰基亚铜[Cu2Cl2(CO)2?2H2O]可知,反应物有:Cu2Cl2、CO、H2O,生成物为[Cu2Cl2(CO)2?2H2O],则反应的化学方程式为:Cu2Cl2+2CO+2H2O═[Cu2Cl2(CO)2?2H2O],故答案为:Cu2Cl2+2CO+2H2O═[Cu2Cl2(CO)2?2H2O];
(2)①金属铜和稀硫酸不反应,但是在鼓入氧气的条件下会发生反应生成硫酸铜,所以A是稀硫酸,B是氧气,
故答案为:稀硫酸;氧气;
②由图示可知,反应物有:Cu2+、SO32-、Cl-,生成物有Cu2Cl2、SO42-,由于是氧化还原反应,化合价发生了变化,根据电子得失和质量守恒进行配平:2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO42-+2H+,在反应②的溶液中加适量稀碱溶液,OH-中和了反应中的H+,有利于平衡向右进行,提高Cu2Cl2的产率,但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了Cu2Cl2的产率,
故答案为:2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO42-+2H+;OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率,但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯;
③根据图象可知,因在55℃时CuCl产率最大,根据信息可知,随温度升高,促进了CuCl的水解,CuCl被氧化的速度加快,
故答案为:55℃;
④根据立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装.真空干燥,密封包装说明氯化亚铜在空气中会被氧化而变质,故答案为:防止氯化亚铜在空气中会被氧化而变质.
(2)①金属铜和稀硫酸不反应,但是在鼓入氧气的条件下会发生反应生成硫酸铜,所以A是稀硫酸,B是氧气,
故答案为:稀硫酸;氧气;
②由图示可知,反应物有:Cu2+、SO32-、Cl-,生成物有Cu2Cl2、SO42-,由于是氧化还原反应,化合价发生了变化,根据电子得失和质量守恒进行配平:2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO42-+2H+,在反应②的溶液中加适量稀碱溶液,OH-中和了反应中的H+,有利于平衡向右进行,提高Cu2Cl2的产率,但当OH-浓度过大时,Cu+能与OH-结合,生成氢氧化亚铜,从而降减了Cu2Cl2的产率,
故答案为:2Cu2++SO32-+2Cl-+H2O=Cu2Cl2↓+SO42-+2H+;OH-中和了反应生成的H+,有利于反应向右进行,提高Cu2Cl2的产率,但当OH-浓度偏大时,Cu2+能与OH结合,生成沉淀,反而降低了Cu2Cl2的产率造成产物不纯;
③根据图象可知,因在55℃时CuCl产率最大,根据信息可知,随温度升高,促进了CuCl的水解,CuCl被氧化的速度加快,
故答案为:55℃;
④根据立即用无水乙醇洗涤,然后真空干燥、冷却,密封包装.真空干燥,密封包装说明氯化亚铜在空气中会被氧化而变质,故答案为:防止氯化亚铜在空气中会被氧化而变质.
点评:本题主要考查了CuCl的制备,对制备过程中的有关知识进行了考查,氧化还原反应实质和规律的应用,培养了学生分析问题的能力和运用知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各种溶液中通入足量的SO2后,既无沉淀又无气体产生的是( )
①NaClO ②C6H5ONa ③Na2S ④BaCl2 ⑤Ba(OH)2 ⑥H2O2.
①NaClO ②C6H5ONa ③Na2S ④BaCl2 ⑤Ba(OH)2 ⑥H2O2.
| A、①④⑥ | B、①②③ |
| C、④⑤⑥ | D、①④⑤⑥ |
下列常见物质的分类不正确的是( )
| A、CO2是酸性氧化物 |
| B、氨水是混合物 |
| C、冰醋酸是电解质 |
| D、纯碱是碱 |
C、N、S都是重要的非金属元素.下列说法正确的是( )
| A、三者对应的氧化物均为酸性氧化物 |
| B、三者的单质直接与氧气反应都能生成两种以上氧化物 |
| C、同温度、同浓度的Na2CO3、NaNO3、Na2SO3溶液的pH:NaNO3<Na2SO3<Na2CO3 |
| D、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
下列关于化学电源的说法不正确的是( )
| A、我们可以根据硫酸密度的大小来判断铅蓄电池是否需要充电 |
| B、燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能转化为热能,然后再转化为电能的化学电源 |
| C、普通锌锰干电池中,发生氧化还原反应的物质大部分被消耗后,就不能再使用了 |
| D、由Ag2O和Zn形成的碱性银锌纽扣电池,发生电化学反应时,Zn作为负极 |
已知R2+核外有a个电子,b个中子.表示R原子符号正确的是( )
| A、R | ||
B、
| ||
C、
| ||
D、
|
下列溶液在空气中加热蒸干并灼烧后,能得到相应溶质固体的是( )
| A、FeCl3 |
| B、KHCO3 |
| C、Fe2(SO4)3 |
| D、FeSO4 |
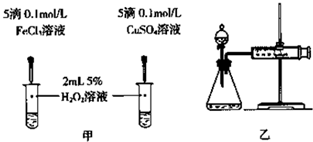
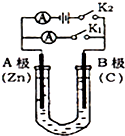 如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的溶液,按要求回答下列问题: