题目内容
13.已知白磷和红磷分别在空气中完全燃烧:?P4(白磷)+5O2(g)→2P2O5(s)+2983.2kJ
?4P(红磷)+5O2(g)→2P2O5(s)+2954kJ
写出红磷转化为白磷的热化学方程式:4P(红磷)→P4(白磷)△H=-29.2KJ/mol.根据该热化学方程式,可推知红磷与白磷相比较,红磷更稳定.
分析 ①P4(白磷)+5O2(g)→2P2O5(s)+2983.2kJ,②?4P(红磷)+5O2(g)→2P2O5(s)+2954kJ,根据盖斯定律②-①可得红磷转化为白磷的热化学方程式;物质具有能量越高,物质的稳定性越弱,据此判断红磷和白磷的稳定性.
解答 解:已知:①P4(白磷)+5O2(g)→2P2O5(s)+2983.2kJ,
②?4P(红磷)+5O2(g)→2P2O5(s)+2954kJ
根据盖斯定律,②-①可得红磷转化为白磷的热化学方程式为:4P(红磷)→P4(白磷)-29.2KJ,
热化学方程式为:4P(红磷)→P4(白磷)△H=-29.2KJ/mol,
该反应为吸热反应,说明红磷具有的能量小于白磷,能量越高稳定性越弱,则红磷更稳定,
故答案为:4P(红磷)→P4(白磷)△H=-29.2KJ/mol;红磷.
点评 本题考查了热化学方程式书写、盖斯定律计算,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
3.下列说法正确的是( )
| A. | 反应热是1 mol物质参加反应时的能量变化 | |
| B. | 当反应放热时△H>0,反应吸热时△H<0 | |
| C. | 任何条件下,化学反应的焓变都等于化学反应的反应热 | |
| D. | 在一定条件下,某一化学反应是吸热反应还是放热反应,由生成物与反应物的焓的差值来决定 |
8.纯净的物质都可以用化学式表示,化学式既可以表示物质分子的实际组成,也可以表示物质中各组成元素的原子个数之比;分子式则只表示物质分子的实际组成.下列化学式中属于分子式的有( )
?①KCl?②SiO2?③C(金刚石)?④CO2?⑤O2⑥?CuSO4?•5H2O⑦?白磷(P4)
?①KCl?②SiO2?③C(金刚石)?④CO2?⑤O2⑥?CuSO4?•5H2O⑦?白磷(P4)
| A. | ???②④⑤⑥ | B. | ????②③④⑤⑦ | C. | ??④⑤⑦ | D. | ???①③⑥ |
5.下列化学用语的表达,正确的是( )
| A. | 氯化氢分子的电子式: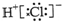 | B. | 乙烯的分子式:C2H6 | ||
| C. | 二氧化碳分子的结构式:O-C-O | D. | CH4分子的球棍模型: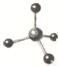 |
3.除去下列各物质中的少量杂质所选用的试剂及操作方法均正确的是( )
| 项目 | 物质 | 杂质(少量) | 试剂 | 操作方法 |
| A | CO2 | SO2 | 饱和NaHCO3溶液 | 洗气 |
| B | 硝酸 | 盐酸 | 过量的AgNO3溶液 | 过滤 |
| C | 溴苯 | 溴 | 加入CCl4 | 分液 |
| D | Na2CO3 | Na2SO4 | 加入适量BaCl2溶液 | 溶解、过滤、洗涤 |
| A. | A | B. | B | C. | C | D. | D |
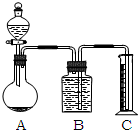 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.
甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验.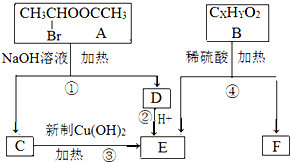 六种有机物之间的转化关系如图.已知:一个碳原子上连有两个羟基的结构极不稳定,易发生变化:R-CH(OH)2→RCHO+H2O
六种有机物之间的转化关系如图.已知:一个碳原子上连有两个羟基的结构极不稳定,易发生变化:R-CH(OH)2→RCHO+H2O
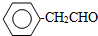 或
或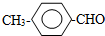 或(邻位、间位).
或(邻位、间位).