题目内容
20.实验室将饱和三氯化铁溶液滴入沸水加热到溶液呈红褐色,请写出反应的化学方程式FeCl3+3H2O=Fe(OH)3(胶体)+3HCl.分析 将饱和三氯化铁溶液滴人沸水中可以制取氢氧化铁胶体,据此写出反应的化学方程式.
解答 解:将饱和的FeCl3溶液逐滴滴入沸水中,液体变为红褐色,得到的是Fe(OH)3胶体,化学方程式为:FeCl3+3H2O=Fe(OH)3(胶体)+3HCl,
故答案为:FeCl3+3H2O=Fe(OH)3(胶体)+3HCl.
点评 本题考查了胶体的性质和制备,熟悉氢氧化铁胶体的制备过程是解题关键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.对于反应:2H2S+SO2═3S+2H2O,被氧化的硫原子与被还原的硫原子的质量之比为( )
| A. | 1:1 | B. | 2:1 | C. | 3:1 | D. | 1:2 |
8.下列描述中正确的是( )
| A. | SO2和SO32-的中心原子均为sp3杂化 | |
| B. | ClO3-的空间构型为三角锥形 | |
| C. | 分子晶体的堆积均采取分子密堆积 | |
| D. | CS2为V形的极性分子 |
15.下列离子方程式中正确的是( )
| A. | 将碳酸钙加入到盐酸中:CO32-+2H+=CO2↑+H2O | |
| B. | 金属钾与水反应:K+H2O=K++OH-+H2↑ | |
| C. | 向稀硝酸中加入少量铜屑:Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| D. | 向偏铝酸钠溶液中通过量CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
12.下列含有非极性键的化合物是( )
| A. | MgCl2 | B. | Na2O2 | C. | H2O | D. | N2 |
15.下列说法中正确的是( )
| A. | 1 mol 丙三醇和足量金属钠反应可以产生 3 mol H2 | |
| B. | 甲苯能使酸性高锰酸钾溶液褪色说明甲基对苯环性质有影响 | |
| C. | 丙烯的二氯代物有 5 种 | |
| D. | 芳香烃的通式是 CnH2n-6 (n≥6,n∈N) |
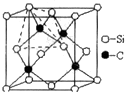 碳、氮、氟、硅、钛等元素的化合物广泛应用于生产生活,回答下列问题:
碳、氮、氟、硅、钛等元素的化合物广泛应用于生产生活,回答下列问题: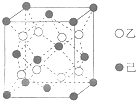 乙、丙、丁简单离子的核外电子排布相同,这三种元素按6:3:1的原子个数比可形成一种离子晶体W;丙与戊可形成常见离子晶体X,甲与己可形成常见离子晶体Y,且X和Y电子数相同.
乙、丙、丁简单离子的核外电子排布相同,这三种元素按6:3:1的原子个数比可形成一种离子晶体W;丙与戊可形成常见离子晶体X,甲与己可形成常见离子晶体Y,且X和Y电子数相同.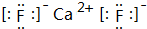 ;
;