题目内容
3.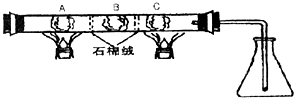 在一硬质玻璃管中进行如图所示的实验,图中A为NH4HCO3,B为Na2O2,C为Pt丝;石棉绒起隔离药品的作用.充分反应后,发现锥形瓶内出现红棕色气体,随之又有白烟产生.
在一硬质玻璃管中进行如图所示的实验,图中A为NH4HCO3,B为Na2O2,C为Pt丝;石棉绒起隔离药品的作用.充分反应后,发现锥形瓶内出现红棕色气体,随之又有白烟产生.(1)C处(Pt为催化剂)发生反应的化学方程式是4NH3+5O2═4NO+6H2O
(2)若在NH4HCO3中预先加入适量的某种药品,再充分反应,可使锥形瓶中仅出现红棕色气体而无白烟,这种药品是b(填编号)
a、NaOH b、NaHCO3 c、NH4Cl.
分析 图中A为NH4HCO3,受热分解产生氨气、水以及二氧化碳,B为Na2O2,可以和水以及二氧化碳反应生成氧气,氨气和氧气在催化剂的作用下会发生反应,据此回答.
解答 解:(1)图中A为NH4HCO3,受热分解产生氨气、水以及二氧化碳,B为Na2O2,可以和水以及二氧化碳反应生成氧气,氨气和氧气在催化剂的作用下会发生反应:4NH3+5O2═4NO+6H2O,即C处(Pt为催化剂)发生反应的化学方程式是:4NH3+5O2═4NO+6H2O,故答案为:4NH3+5O2═4NO+6H2O;
(2)若在NH4HCO3中预先加入适量的某种药品,再充分反应,可使锥形瓶中仅出现红棕色气体而无白烟,则所加的物质加热下,可以产生和氨气反应的 产物,只能是b.
故选b.
点评 本题考查学生铵盐的性质,注意知识的迁移应用是关键,难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
11.图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为 .
.
(2)地壳中含量最多的金属元素是Al.写出元素⑥的最简单氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③、④、⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑤与氢氧化钠溶液反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al.写出元素⑥的最简单氢化物的化学式CH4.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出③、④、⑤对应离子氧化性由强到弱的是Al3+>Mg2+>Na+,②、⑦、⑩对应氢化物酸性由强到弱的是HBr>HCl>HF.
(5)写出⑤与氢氧化钠溶液反应的化学方程式:2Al+2NaOH+2H2O═2NaAlO2+3H2↑..
18.下列各离子组中,能在水溶液中大量共存,当滴加稀硫酸后则不能大量共存的是( )
| A. | Na+、Mg2+、Cl-、I- | B. | Fe2+、Ba2+、S2-、Cl- | ||
| C. | Na+、Al3+、Cl-、HCO3- | D. | K+、Fe2+、Cl-、NO3- |
8.下列各组物质中,气体X和气体Y同时通入盛有溶液Z的洗气瓶中,一定没有沉淀生成的是( )
| X | Y | Z | |
| A | Cl2 | SO2 | BaCl2 |
| B | NH3 | O2 | Al2(SO4)3 |
| C | NH3 | CO2 | MgCl2 |
| D | CO2 | SO2 | CaCl2 |
| A. | A | B. | B | C. | C | D. | D |