题目内容
(10)氧族元素的各种性质可归纳整理如下(部分):
| 元素 性质 | 8O | 16S | Se | 52Te |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径(nm) | 0.074 | 0.102 | 0.116 | 0.143 |
| 单质与H2反应 | 点燃易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)氧离子的结构示意图为 ,硫离子的电子式为 。
(2)碲的主要化合价可能有 。
(3)氧元素比硫无素非金属性 (填强和弱)。请用化学方程式证明该结论:
(4)H2O2可以作脱氯剂,用于消除水中的Cl2,写出该反应的化学方程式:
(1)  [ S ]2- (2)-2.、+4、+6
[ S ]2- (2)-2.、+4、+6
(3)强 O2+2H2S="2S" +2H2O (4)Cl2+H2O2=2HCl+O2
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
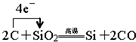
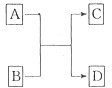 (2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题:
(2013?江西模拟)(一)X、Y、Z、L、M五种元素的原子序数依次增大,X的阴离子与Y的内层电子数相等,Y原子的最外层电子数是次外层电子数的两倍,Z、L是空气中含量最多的二种元素,M是地壳中含量最高的金属元素.回答下列问题: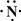 →
→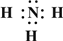

 N2O4(g);△H<0。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。
N2O4(g);△H<0。在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如下图所示。

