题目内容
X、Y、Z、W为四种短周期元素.X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价的代数和为6;Z在地壳中的含量仅次于氧;Y、Z、W同周期,W的常见化合价为+3.回答下列问题:
(1)Y是
O
O;
(3)Z 的最高价氧化物与Z 同主族的单质A能发生置换反应,这个反应在工业上是获得Z 的一步重要反应.写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目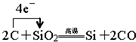
 ;
;
(4)用惰性电极电解由Y、W两种元素组成的化合物的溶液,写出阳极电极反应式
(5)Y的气态氢化物与氨气反应的生成物溶于水,其溶液显
(1)Y是
Cl(或氯)
Cl(或氯)
; (2)写出含有10个中子X原子的原子符号18 8 |
18 8 |
(3)Z 的最高价氧化物与Z 同主族的单质A能发生置换反应,这个反应在工业上是获得Z 的一步重要反应.写出该步反应的化学方程式,并用单线桥法标出电子转移的方向与数目


(4)用惰性电极电解由Y、W两种元素组成的化合物的溶液,写出阳极电极反应式
2Cl--2e-=Cl2↑
2Cl--2e-=Cl2↑
;(5)Y的气态氢化物与氨气反应的生成物溶于水,其溶液显
酸
酸
性,溶液中各离子浓度大小关系c(Cl-)>c(NH4+)>c(H+)>c(OH-)
c(Cl-)>c(NH4+)>c(H+)>c(OH-)
.分析:X、Y、Z、W为四种短周期元素.X原子最外层电子数是核外电子层数的3倍,则X的电子层数为2,最外层电子为6,所以X为O;Y最高正价与最低负价的代数和为6,其最高正价为+7,所以Y为Cl;Z在地壳中的含量仅次于氧,即Z为Si;Y、Z、W同周期,W的常见化合价为+3,所以W为第三周期第ⅢA族元素,即W为Al,然后结合元素及其单质、化合物的性质来解答.
解答:解:X、Y、Z、W为四种短周期元素.X原子最外层电子数是核外电子层数的3倍,则X的电子层数为2,最外层电子为6,所以X为O;Y最高正价与最低负价的代数和为6,其最高正价为+7,所以Y为Cl;Z在地壳中的含量仅次于氧,即Z为Si;Y、Z、W同周期,W的常见化合价为+3,所以W为第三周期第ⅢA族元素,即W为Al,
(1)由以上分析可知,Y为Cl(或氯),故答案为:Cl(或氯);
(2)X为O,质子数为8,中子数为10,则质量数为18,该原子为
O,故答案为:
O;
(3)二氧化硅与C反应生成硅和CO,该反应中转移4e-,用单线桥法标出电子转移的方向与数目为 ,
,
故答案为:; ;
;
(4)惰性电极电解由Y、W两种元素组成的MgCl2的溶液,在阳极氯离子放电,电极反应为2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
(5)Y的气态氢化物与氨气反应的生成物为氯化铵,铵根离子水解显酸性,该溶液中离子浓度的关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:酸;c(Cl-)>c(NH4+)>c(H+)>c(OH-).
(1)由以上分析可知,Y为Cl(或氯),故答案为:Cl(或氯);
(2)X为O,质子数为8,中子数为10,则质量数为18,该原子为
18 8 |
18 8 |
(3)二氧化硅与C反应生成硅和CO,该反应中转移4e-,用单线桥法标出电子转移的方向与数目为
 ,
,故答案为:;
 ;
;(4)惰性电极电解由Y、W两种元素组成的MgCl2的溶液,在阳极氯离子放电,电极反应为2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
(5)Y的气态氢化物与氨气反应的生成物为氯化铵,铵根离子水解显酸性,该溶液中离子浓度的关系为c(Cl-)>c(NH4+)>c(H+)>c(OH-),
故答案为:酸;c(Cl-)>c(NH4+)>c(H+)>c(OH-).
点评:本题考查位置、结构、性质的关系及应用,元素的推断是解答本题的关键,并熟悉元素化合物的性质、氧化还原反应、电解、水解等知识来解答,综合性较强,题目难度中等.

练习册系列答案
相关题目
 NH3?H2O+H+
NH3?H2O+H+ H++HO2-HO2-
H++HO2-HO2- H++O22-
H++O22-