题目内容
某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.为此,他们设计了如图装置验证所产生的气体成分.
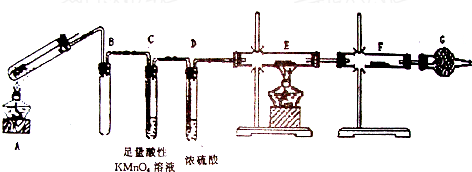
(1)装置中的药品名称或化学式:E ,F ;装置的作用:C ,G .
(2)先点燃 处酒精灯(填“A”或“E”),点燃E处酒精灯前一步操作是 ,E中发生的反应方程式为 .
(3)反应后A的溶液中含有Fe3+和Fe2+,检验其中的Fe2+的方法是 .

(1)装置中的药品名称或化学式:E
(2)先点燃
(3)反应后A的溶液中含有Fe3+和Fe2+,检验其中的Fe2+的方法是
考点:浓硫酸的性质实验,铁及其化合物的性质实验
专题:实验题
分析:(1)E处装置是为了验证是否有氢气生成,故利用氢气还原氧化铜进行验证;无水硫酸铜遇水变蓝色;酸性高锰酸钾溶液能和二氧化硫发生反应而褪色;空气中的H2O会进入F产生影响;
(2)A装置中酒精灯的作用是使浓硫酸和铁反应生成二氧化硫,氢气和氧化铜的反应中要检验氢气的纯度,否则后产生安全事故,氢气与氧化铜反应生成铜单质和水;
(3)亚铁离子能使酸性高锰酸钾溶液褪色.
(2)A装置中酒精灯的作用是使浓硫酸和铁反应生成二氧化硫,氢气和氧化铜的反应中要检验氢气的纯度,否则后产生安全事故,氢气与氧化铜反应生成铜单质和水;
(3)亚铁离子能使酸性高锰酸钾溶液褪色.
解答:
解:(1)铁与稀硫酸反应会产生氢气,故此实验E处应加入试剂CuO,利用氢气还原氧化铜的性质生成水来验证氢气的存在,F处是验证水的存在,常用水能使无水硫酸铜变蓝这一性质;酸性高锰酸钾溶液有强氧化性,二氧化硫能和酸性高锰酸钾溶液发生氧化还原反应而使其褪色,所以酸性高锰酸钾的作用是:验证有SO2生成,同时除去SO2;空气中含有水蒸气,如果没有G装置,水蒸气进入F装置干扰实验,所以G的作用是:防止空气中的H2O进入F,
故答案为:Cu0;无水硫酸铜;验证有SO2生成,同时除去SO2;防止空气中的H2O进入F;
(2)A装置的目的是制取气体,E装置的目的是检验生成的气体,所以先点燃A处酒精灯;氢气是可燃性气体,在一定范围内易产生爆炸,为防止安全事故产生所以点燃E处酒精灯前一步操作是:检验氢气的纯度,氢气与氧化铜在加热的条件下反应生成铜单质和水,
故答案为:A;在G处收集气体并检验纯度,CuO+H2
Cu+H2O;
(3)酸性高锰酸钾有强氧化性,能氧化二氧化硫而使其褪色,所以检验亚铁离子的方法是:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+,
故答案为:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+.
故答案为:Cu0;无水硫酸铜;验证有SO2生成,同时除去SO2;防止空气中的H2O进入F;
(2)A装置的目的是制取气体,E装置的目的是检验生成的气体,所以先点燃A处酒精灯;氢气是可燃性气体,在一定范围内易产生爆炸,为防止安全事故产生所以点燃E处酒精灯前一步操作是:检验氢气的纯度,氢气与氧化铜在加热的条件下反应生成铜单质和水,
故答案为:A;在G处收集气体并检验纯度,CuO+H2
| ||
(3)酸性高锰酸钾有强氧化性,能氧化二氧化硫而使其褪色,所以检验亚铁离子的方法是:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+,
故答案为:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+.
点评:本题考查了常见气体的制备原理及其性质,难度不大,明确二氧化硫的性质是解本题的关键,注意亚铁离子、铁离子的检验方法是高考的热点,是学习的重点.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
下列物质的水溶液能导电,但它属于非电解质的是( )
| A、CO2 |
| B、Na2CO3 |
| C、HCl |
| D、Cl2 |
在一定温度下,向容积固定不变的密闭容器里充入a mol N2O4发生如下反应:N2O4 (气)?2NO2 (气),达到平衡后,再向该容器内充入a mol N2O4,达平衡后与原平衡比较正确的是( )
| A、平均相对分子质量增大 |
| B、N2O4的转化率提高 |
| C、压强为原来的2倍 |
| D、颜色变深 |
下列关于离子的检验正确的是( )
| A、往溶液中加入BaCl2溶液,有白色沉淀生成说明一定有SO42- |
| B、向待测溶液中加入盐酸,产生无色无味可使澄清石灰水变浑浊的气体,则一定存在大量CO32- |
| C、往待测溶液中加入氯水然后再滴加KSCN溶液,溶液变红,证明一定有Fe3+ |
| D、向待测溶液中加硝酸酸化的AgNO3溶液,有白色沉淀产生,证明有Cl- |
1体积pH=2的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( )
| A、8.0 | B、9.0 |
| C、10.0 | D、11.0 |