题目内容
下列关于离子的检验正确的是( )
| A、往溶液中加入BaCl2溶液,有白色沉淀生成说明一定有SO42- |
| B、向待测溶液中加入盐酸,产生无色无味可使澄清石灰水变浑浊的气体,则一定存在大量CO32- |
| C、往待测溶液中加入氯水然后再滴加KSCN溶液,溶液变红,证明一定有Fe3+ |
| D、向待测溶液中加硝酸酸化的AgNO3溶液,有白色沉淀产生,证明有Cl- |
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:A、向一种未知溶液中加入BaCl2溶液,有白色沉淀生成,沉淀可能是AgCl或BaSO4沉淀;
B、无色无味的可使澄清石灰水变浑浊的气体为二氧化碳,碳酸根、碳酸氢根均能与酸反应生成二氧化碳;
C、氯水具有强氧化性,能氧化亚铁离子生成铁离子;
D、排除碳酸根等的干扰可以验证Cl-的存在.
B、无色无味的可使澄清石灰水变浑浊的气体为二氧化碳,碳酸根、碳酸氢根均能与酸反应生成二氧化碳;
C、氯水具有强氧化性,能氧化亚铁离子生成铁离子;
D、排除碳酸根等的干扰可以验证Cl-的存在.
解答:
解:A、向一种未知溶液中加入BaCl2溶液,有白色沉淀生成,沉淀可能是AgCl或BaSO4沉淀,溶液中可能含有Cl-或SO42-离子,故A错误;
B、碳酸根、碳酸氢根均能与酸反应生成二氧化碳气体,故B错误;
C、氯水能氧化亚铁离子为铁离子,故C错误;
D、某溶液中加入硝酸酸化的硝酸银生成白色沉淀,说明该溶液中含有氯离子,故D正确,故选D.
B、碳酸根、碳酸氢根均能与酸反应生成二氧化碳气体,故B错误;
C、氯水能氧化亚铁离子为铁离子,故C错误;
D、某溶液中加入硝酸酸化的硝酸银生成白色沉淀,说明该溶液中含有氯离子,故D正确,故选D.
点评:本题考查物质的检验、鉴别、反应现象的判断,解题关键是干扰离子的分析判断,题目难度中等.

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
核外电子数相等的原子一定是( )
①同种元素②同种核素③质子数相同④质量数相同⑤中子数相同⑥最外层电子数相同.
①同种元素②同种核素③质子数相同④质量数相同⑤中子数相同⑥最外层电子数相同.
| A、①②③⑤ | B、①③⑥ |
| C、①③④⑥ | D、全部 |
下列有关溶液配制说法错误的是( )
| A、称取12.5g胆矾[CuSO4?5H2O]溶于水中,并加水稀释至500mL,所得溶液物质的量浓度为0.1mol?L-1 |
| B、取58.5gNaCl固体放入1L水中充分溶解,所得溶液中NaCl的物质的量浓度为1mol?L-1 |
| C、将100g 5%的食盐水加热蒸发掉50g水后,所得溶液中NaCl的质量分数为10% |
| D、将浓度为2 mol?L-1硫酸钠溶液10mL加水稀释至200mL,所得溶液浓度为0.1mol?L-1 |
根据下列化学实验事实得出的结论一定正确的是( )
| A、向某无色溶液中先加入氯化钡溶液,生成白色沉淀,再加入足量盐酸,沉淀不溶解.结论:该溶液中有SO42- |
| B、向某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝.结论:该溶液中有NH4+ |
| C、向1 mL浓度均为0.05 mol?L-1的NaCl、NaI混合溶液中滴加2滴0.01 mol?L-1的AgNO3溶液,振荡,沉淀呈黄色. 结论:Ksp(AgCl)<Ksp(AgI) |
| D、向1 mL 1%的NaOH溶液中加入2 mL 2%的CuSO4溶液,振荡后再加入0.5 mL有机物X,加热后未出现红色沉淀.结论:X中不含有醛基 |
分别往含有下列离子的溶液中通入氯气,离子浓度不会减少的是( )
| A、H+ |
| B、HC03- |
| C、OH- |
| D、Ag+ |
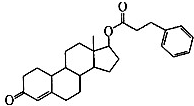 苯丙酸诺龙是一种兴奋剂,结构简式为:
苯丙酸诺龙是一种兴奋剂,结构简式为: