题目内容
15.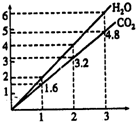 两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )
两种气态烃组成的混合气体,完全燃烧后得到C02和H2O的物质的量随着混合烃物质的量的变化如图所示.则下列对混合烃的判断正确的是( )| A. | 一定含有CH4 | B. | 一定含有C2H6 | C. | 一定含有C2H4 | D. | 一定不含有C3H4 |
分析 由图可知,1体积混合气体完全燃烧生成1.6体积二氧化碳气体和2体积水,则两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,碳原子数目大于1.6,不超过4,据此判断.
解答 解:由图可知两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,由氢原子平均数可知,另一气态烃中氢原子数目为4,碳原子数目大于1.6,不超过4,可能含有C2H4、C3H4,
A.两种气态烃的平均组成为C1.6H4,根据碳原子平均数可知,混合气体一定含有CH4,故A正确;
B.C2H6中氢原子数目为6,氢原子数目大于4,所有不可能含有C2H6,故B错误;
C.可能含有C2H4、C3H4,则不一定含有C2H4,故C错误;
D.含有可能含有C2H4、C3H4,故D错误;
故选A.
点评 本题考查烃混合物分子式确定,题目难度中等,利用图象数据正确推断该混合烃的平均分子式为解答关键,注意掌握平均分子式中确定有机物分子组成中的应用方法.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
6.将纯水加热至较高温度,下列叙述正确的是( )
| A. | Kw变大、pH变小、呈酸性 | B. | Kw变大、pH不变、呈中性 | ||
| C. | Kw变小、pH变大、呈碱性 | D. | Kw变大、pH变小、呈中性 |
10.CH3COOH分别跟H-18O-C2H5和H-16O-C2H5起酯化反应后,两者生成水的质量( )
| A. | 前者大 | B. | 前者小 | C. | 相等 | D. | 不能确定 |
20.镁、铝混合粉末10.2g溶于500mL 4mol/L盐酸中.若加入2mol/L的氢氧化钠溶液,使得沉淀达到最大量,则需加入氢氧化钠溶液的体积为( )
| A. | 100 mL | B. | 500 mL | C. | 1000 mL | D. | 1500 mL |
7.下列说法正确的是( )
| A. | 可用丁达尔现象区分溶液与胶体 | |
| B. | 生石灰与水混合的过程只发生物理变化 | |
| C. | O3是由3个氧原子构成的化合物 | |
| D. | CuSO4•5H2O是一种混合物 |
15.亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,常用于水的消毒以及纺织高漂白.过氧化氢法生产亚氯酸钠的流程图如下
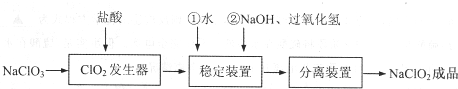
已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O且NaClO2在碱性条件下稳定性较高.试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O.
(2)在稳定装置中生成NaClO2,H2O2作B(选填序号).
A.氧化剂 B.还原剂 C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
反应生成NaClO2的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.
(3)在实验室模拟“固体分离装置”中的技术(即从溶液中分离出溶质),必须进行的实验操作是BEA(按实验先后顺序填写操作代号).
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却 F.萃取
(4)经查阅资料知道:①当pH≤2.0时,ClO2-能被I-完全还原成Cl-;
②溶液中能发生反应:2S2O32-+I2=2I-+S4O62-.
欲测定成品中NaClO2的含量,现进行如下操作:
①步骤Ⅱ中发生反应的离子方程式是ClO2-+4H++4I-=2I2+Cl-+2H2O,
②步骤Ⅲ中达到滴定终点时的现象是滴入最后一滴标准溶液,溶液由蓝色变化为无色且半分钟不变化.
若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数$\frac{9.05×10{\;}^{-2}VC}{4W}$(用有关字母表示).
(5)ClO2是新型饮用水消毒剂,Cl2常用于饮用水消毒.等物质的量的物质,ClO2的消毒效率是Cl2的2.5倍.

已知NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O且NaClO2在碱性条件下稳定性较高.试回答下列问题:
(1)在ClO2发生器中同时有氯气产生,则在发生器中发生反应的化学方程式为2NaClO3+4HCl=2NaCl+2ClO2↑+Cl2↑+2H2O.
(2)在稳定装置中生成NaClO2,H2O2作B(选填序号).
A.氧化剂 B.还原剂 C.既作氧化剂又作还原剂 D.既不作氧化剂也不作还原剂
反应生成NaClO2的化学方程式为2NaOH+2ClO2+H2O2=2NaClO2+2H2O+O2.
(3)在实验室模拟“固体分离装置”中的技术(即从溶液中分离出溶质),必须进行的实验操作是BEA(按实验先后顺序填写操作代号).
A.过滤 B.加热 C.分液 D.蒸馏 E.冷却 F.萃取
(4)经查阅资料知道:①当pH≤2.0时,ClO2-能被I-完全还原成Cl-;
②溶液中能发生反应:2S2O32-+I2=2I-+S4O62-.
欲测定成品中NaClO2的含量,现进行如下操作:
| 步骤Ⅰ | 称取NaClO2样品Wg,加水配成溶液置于锥形瓶中,并调节pH≤2.0 |
| 步骤Ⅱ | 向锥形瓶中加入足量KI晶体,充分搅拌,并加入少量指示剂 |
| 步骤Ⅲ | 用c mol•L-1的 Na2S2O3溶液滴定 |
②步骤Ⅲ中达到滴定终点时的现象是滴入最后一滴标准溶液,溶液由蓝色变化为无色且半分钟不变化.
若上述滴定操作中用去了V mL Na2S2O3溶液,则样品中NaClO2的质量分数$\frac{9.05×10{\;}^{-2}VC}{4W}$(用有关字母表示).
(5)ClO2是新型饮用水消毒剂,Cl2常用于饮用水消毒.等物质的量的物质,ClO2的消毒效率是Cl2的2.5倍.
16.已知25℃时,电离平衡常数Ka(HF)=3.6×10-4 mol/L,溶度积常数Ksp(CaF2)=1.46×10-10 mol3/L3.现向1L 0.2mol/L HF溶液中加入1L 0.2mol•L-1 CaCl2溶液,则下列说法中,正确的是( )
| A. | 25℃时,0.1 mol/L HF溶液中pH=1 | |
| B. | Ksp(CaF2)随温度和浓度的变化而变化 | |
| C. | 该体系中,Ksp(CaF2)=$\frac{1}{{K}_{a}HF}$ | |
| D. | 该体系中有CaF2沉淀产生 |
 ,C02的结构式为O=C=O.
,C02的结构式为O=C=O.