题目内容
下列叙述的两个量,一定相等的是( )
| A、等质量的铝分别与盐酸和氢氧化钠溶液反应生成氢气的物质的量 |
| B、1 mol/L KI与0.5 mol/L K2CO3溶液中的K+数目 |
| C、质量比为3:4的金刚石和石墨中的碳碳键数目 |
| D、常温下,pH均为3的HNO3与Fe(NO3)3溶液中,由水电离产生的c(H+) |
考点:铝的化学性质,物质的量浓度,金刚石、二氧化硅等原子晶体的结构与性质的关系,盐类水解的应用
专题:基本概念与基本理论
分析:A、根据有关反应方程式:2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑来回答;
B、溶液中的离子数目N=nNA=cVNA,据此回答;
C、根据金刚石和石墨中化学键的有关情况来计算;
D、HNO3对水的电离起到抑制作用,Fe(NO3)3水解对水的电离起到促进作用.
B、溶液中的离子数目N=nNA=cVNA,据此回答;
C、根据金刚石和石墨中化学键的有关情况来计算;
D、HNO3对水的电离起到抑制作用,Fe(NO3)3水解对水的电离起到促进作用.
解答:
解:A、根据反应方程式:2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑,当酸碱足量时,等质量的铝分别与盐酸和氢氧化钠溶液反应生成氢气的物质的量才相等,故A错误;
B、不知道溶液的体积,无法计算溶液中离子的数目,故B错误;
C、金刚石是正四面体结构,平均每两个碳原子右两个碳碳键,石墨是六边形结构,每个环有两个碳原子,三个碳碳键,平均每个碳原子有1.5个碳碳键,质量比为3:4的金刚石和石墨,物质的量之比是3:4,含有的碳碳键为(3×2):(4×1.5)=1:1,故C正确;
D、HNO3对水的电离起到抑制作用,Fe(NO3)3水解对水的电离起到促进作用,pH均为3的HNO3与Fe(NO3)3溶液中,由水电离产生的c(H+)不相等,故D错误.
故选C.
B、不知道溶液的体积,无法计算溶液中离子的数目,故B错误;
C、金刚石是正四面体结构,平均每两个碳原子右两个碳碳键,石墨是六边形结构,每个环有两个碳原子,三个碳碳键,平均每个碳原子有1.5个碳碳键,质量比为3:4的金刚石和石墨,物质的量之比是3:4,含有的碳碳键为(3×2):(4×1.5)=1:1,故C正确;
D、HNO3对水的电离起到抑制作用,Fe(NO3)3水解对水的电离起到促进作用,pH均为3的HNO3与Fe(NO3)3溶液中,由水电离产生的c(H+)不相等,故D错误.
故选C.
点评:本题涉及金属铝的性质、物质的量浓度的计算公式的应用、物质的结构、盐的水解原理的应用知识,属于综合知识的考查,难度中等.

练习册系列答案
相关题目
下列不饱和化合物(单体)能在一定条件下发生加聚反应生成如图所示物质的是:( )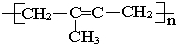
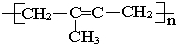
| A、丙烯 |
| B、2-甲基-1,3-丁二烯 |
| C、乙烯和丙烯 |
| D、2-甲基-2-丁烯 |
分子式为C10H14的烃,有一个苯环、两个取代基,其可能的结构有( )
| A、3种 | B、6种 | C、7种 | D、9种 |
将2mol A和1mol B充入某密闭容器中发生反应:2A(g)+B(g)?xC(g),达到化学平衡后,C的体积分数为a.假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是(双选)( )
| A、若在恒温恒压下,当x=1时,按1.5 mol A、1 mol C作为起始物质,达到平衡后,C的体积分数仍为a |
| B、若在恒温恒容下,当x=2时,将2molC作起始物质,达到平衡后,C的体积分数仍为a |
| C、若在恒温恒压下,当x=3时,1mol A、1mol B、6mol C作起始物质,达到平衡后,C的体积分数仍为a |
| D、若在恒温恒容下,按0.6mol A、0.3mol B、1.4mol C作起始物质,达到平衡后,C的体积分数仍为a,则x一定为2或3 |
下列混合物分离(或除杂)的方法正确的是( )
| A、除去Mg粉中的Al粉:加入足量NaOH溶液后,过滤、洗涤 |
| B、除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤 |
| C、除去NaHCO3溶液中Na2CO3:加适量稀盐酸 |
| D、除去Fe2O3中的少量Al2O3:加入过量氢氧化钠溶液,过滤,洗涤 |
在一固定体积的密闭容器中,加入2mol SO2和1mol O2发生反应2SO2(g)+O2(g)?2SO3(g),达到平衡时,SO2的浓度为w mol/L.若维持容器体积和温度不变,以下列四种配比作为起始物质,达平衡后,SO2的浓度仍为w mol/L的是( )
| A、4mol SO2+2mol O2 |
| B、1mol SO2+1mol O2 |
| C、1mol SO2+1mol O2+1mol SO3 |
| D、1mol SO2+0.5mol O2+1mol SO3 |
在体积恒定的密闭容器中,充入3molA和1molB发生反应:3A(g)+B(g)?xC(g),达平衡后,C在平衡混合气中的体积分数为w.若维持稳定不变,按1.2molA、0.4molB、0.6molC为起始物质,达平衡后压强不变,C的体积分数仍为w,则x的值为( )
| A、1 | B、2 | C、4 | D、1或4 |
有关甲烷和丙烷的说法中,错误的是( )
| A、互为同系物 |
| B、均不能使高锰酸钾酸性溶液褪色 |
| C、等质量燃烧消耗氧气甲烷多 |
| D、甲烷没有同分异构体而丙烷有两种同分异构体 |
0.1mol/L CH3COONa稀溶液中,下列离子浓度关系不正确的是( )
| A、c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| B、c(Na+)>c(CH3COO-)>c (OH-)>c(H+) |
| C、c(CH3COO- )+c(CH3COOH)=0.1 mol/L |
| D、c(Na+)>c(CH3COO-)>c (H+)>c(OH-) |