题目内容
2.1774年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.现将17.4gMnO2与200克36.5%的浓盐酸完全反应,回答下列问题(要有计算过程并要求取三位有效数字):(1)反应中被还原的物质是什么?
(2)生成的Cl2的体积(标准状况)是多少?
(3)求反应中被氧化的HCl的物质的量.
分析 (1)元素化合价降低,发生还原反应;
(2)计算可知HCl过量,MnO2完全反应,根据二氧化锰的量计算生成氯气体积;
(3)被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl物质的量.
解答 解:(1)反应中MnO2中Mn元素化合价降低,则被还原的物质为MnO2,
答:被还原的物质为MnO2.
(2)n(MnO2)=$\frac{17.4g}{87g/mol}$=0.200mol,n(HCl)=$\frac{200g×36.5%}{36.5g/mol}$=2.00mol,由方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,可知HCl过量,则n(Cl2)=n(MnO2)=0.2mol,故标况下生成氯气的体积为0.200mol×22.4L/mol=4.48L,
答:标况下生成氯气体积为4.48L.
(3)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl物质的量为0.200mol×2=0.400mol,
答:被氧化HCl物质的量为0.400mol,
点评 本题考查氧化还原反应及计算、化学方程式计算,比较基础,有利于基础知识的巩固.

练习册系列答案
相关题目
12.下列离子方程式正确的是( )
| A. | 向明矾溶液中加入氢氧化钡溶液至沉淀的物质的量达到最大值:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| B. | 向澄清石灰水中通入少量CO2:OH-+CO2═HCO3- | |
| C. | 醋酸溶液与水垢中的CaCO3反应:CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ | |
| D. | 硝酸银溶液中加入铜粉:Ag++Cu═Cu2++Ag |
13.下列各组物质按单质、电解质、混合物的顺序排列正确的是( )
| A. | 空气,熟石灰,盐酸 | B. | 青铜,纯碱,水玻璃 | ||
| C. | 石英,二氧化硫,硫酸 | D. | 液氯,烧碱,漂白粉 |
17.将一小块钠放入下列溶液时,不会出现沉淀的是( )
| A. | 氯化镁溶液 | B. | 饱和氢氧化钠溶液 | ||
| C. | 硫酸铜溶液 | D. | 稀硫酸 |
7.含浓度均为0.1mol/L的硫酸、硫酸铜的混合溶液200mL,加入一定质量的锌片,生成气体224mL(标准状况下),则加入锌片的质量为( )
| A. | 1.95g | B. | 0.65g | C. | 2.6g | D. | 1.3g |
14.下列化学用语表达正确的是( )
①丙烷的球棍模型: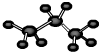
②丙烯的结构简式为:CH3CHCH2
③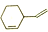 的化学式为C8H12
的化学式为C8H12
④一氯甲烷和二氯甲烷、乙烯和苯乙烯互为同系物
⑤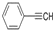 与C8H6互为同分异构体
与C8H6互为同分异构体
⑥石油是混合物,其分馏产品煤油为纯净物.
①丙烷的球棍模型:

②丙烯的结构简式为:CH3CHCH2
③
 的化学式为C8H12
的化学式为C8H12 ④一氯甲烷和二氯甲烷、乙烯和苯乙烯互为同系物
⑤
 与C8H6互为同分异构体
与C8H6互为同分异构体⑥石油是混合物,其分馏产品煤油为纯净物.
| A. | ①③④⑤ | B. | ①③ | C. | ②④⑥ | D. | ①② |
11.下列现象说明SO2具有氧化性的是( )
| A. | SO2通入酸性高锰酸钾溶液中使之褪色 | |
| B. | SO2通入石蕊试液中使之变红色 | |
| C. | SO2通入氯水中使之褪色 | |
| D. | SO2通入饱和H2S溶液中析出浅黄色沉淀 |
7.X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素.三种元素相互之间可以形成1:1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是( )
| A. | 三种元素形成的离子半径与原子半径大小顺序相同 | |
| B. | Z是地壳中含量最多的元素 | |
| C. | M、N、R晶体类型相同 | |
| D. | 少量M、N投入水中所得溶液的溶质相同 |


 .
.