题目内容
14.常温下能发生反应的一组气体是( )| A. | N2、O2 | B. | NO、O2 | C. | H2、O2 | D. | H2、CO |
分析 A、氮气和氧气在放电条件下反应;
B、一氧化氮与氧气在常温下反应生成二氧化氮;
C、氢气与氧气在点燃条件下反应生成水;
D、氢气与一氧化碳常温下不反应.
解答 解:A、氮气和氧气在放电条件下反应,在常温下不反应,故A错误;
B、一氧化氮与氧气在常温下反应生成二氧化氮,所以符合条件,故B正确;
C、氢气与氧气在点燃条件下反应生成水,在常温下不反应,故C错误;
D、氢气与一氧化碳常温下不反应,不符合条件,故D错误;
故选B.
点评 本题考查了物质间的反应,明确物质的性质是解本题关键,根据物质的性质来分析解答,总结归纳元素化合物知识,灵活运用知识解答问题,题目难度不大.

练习册系列答案
相关题目
9.室温下,下列各组离子在指定溶液中,一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、Fe2+、NO3-、SO42- | |
| B. | 水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Al3+、Cl-、SO42- | |
| C. | 加入酚酞溶液显红色的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 无色溶液中:K+、NH4+、Cl-、NO3- |
5.常温下,不溶于浓H2SO4,也不溶于浓HNO3和浓NaOH溶液的金属是( )
| A. | 铁 | B. | 钠 | C. | 镁 | D. | 铜 |
2.实验中的下列操作正确的是( )
| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多,为不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 |
9.下列有关物质相互转化的说法正确的是( )
| A. | 石墨转变成碳纳米管为物理变化 | |
| B. | “滴水石穿,绳锯木断”不包含化学变化 | |
| C. | 232Th转化为233U是化学变化 | |
| D. | 将地沟油制成肥皂是化学变化 |
6.90%的硫酸与10%的硫酸等体积混合,所得溶液的质量分数为( )
| A. | 等于50% | B. | 大于50% | C. | 小于50% | D. | 无法确定 |
3.下列实验现象可用同一原理解释的是( )
| A. | 品红溶液中分别通入SO2和Cl2,品红均褪色 | |
| B. | 鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出 | |
| C. | 分别加热盛有NH4Cl和单质碘的试管,管口均有固体凝结 | |
| D. | 溴水分别滴入植物油和裂化汽油中,溴水均褪色 |
4.设NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 标况下,4.48L氦气和重氢气的混合物中含中子数为0.4NA | |
| B. | 在含有4molSi-O键的石英晶体中,氧原子数目为2 NA | |
| C. | 7.8克过氧化钠中,所含阴、阳离子总数为0.4NA | |
| D. | 28克N60单质中(如图),含的N-N键(σ键)个数为3 NA |
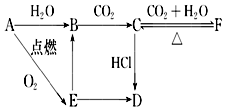 A、B、C、D、E、F六种含有相同元素的物质有如图变化关系,E是淡黄色粉末:
A、B、C、D、E、F六种含有相同元素的物质有如图变化关系,E是淡黄色粉末: