题目内容
下列表示对应化学反应的离子方程式正确的是( )
A、MnO2 与浓盐酸反应制Cl2:MnO2+4HCl
| ||||
| B、明矾溶于水产生Al(OH)3 胶体:Al3++3H2O═Al(OH)3↓+3H+ | ||||
| C、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | ||||
| D、Na2O2 溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.浓盐酸中的氯化氢在离子方程式中应该拆开,不能保留分子式;
B.氢氧化铝胶体,不能表示为氢氧化铝沉淀,且为可逆反应,不能用等号;
C.氢氧化钠溶液少量,离子方程式按照氢氧化钠的组成书写;
D.过氧化钠与氧气的计量数关系错误,违反了电子守恒.
B.氢氧化铝胶体,不能表示为氢氧化铝沉淀,且为可逆反应,不能用等号;
C.氢氧化钠溶液少量,离子方程式按照氢氧化钠的组成书写;
D.过氧化钠与氧气的计量数关系错误,违反了电子守恒.
解答:
解:A.MnO2与浓盐酸反应制Cl2,氯化氢应该拆开,正确的离子方程式为:MnO2+2Cl-+4H+
Mn2++Cl2↑+2H2O,故A错误;
B.明矾溶于水产生Al(OH)3 胶体,不能用等号和沉淀符号,正确的离子方程式为:Al3++3H2O?Al(OH)3+3H+,故B错误;
C.Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙沉淀和水,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故D错误;
故选C.
| ||
B.明矾溶于水产生Al(OH)3 胶体,不能用等号和沉淀符号,正确的离子方程式为:Al3++3H2O?Al(OH)3+3H+,故B错误;
C.Ca(HCO3)2溶液与少量NaOH溶液反应生成碳酸钙沉淀和水,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,正确的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故D错误;
故选C.
点评:本题考查了离子方程式的书写判断,题目难度中等,注意掌握离子方程式的书写原则,明确常见的难溶物、弱电解质、气体等需要保留化学式的物质名称,注意反应物过量时,离子方程式按照不足量的化学式组成书写.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目
有关化学用语的表示正确的是( )
| A、HCN分子的结构式:H-C≡N |
B、二氧化碳的电子式: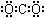 |
C、Cl-的结构示意图为: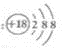 |
| D、乙烯的结构简式为CH2CH2 |
下列电离方程式的书写正确的是( )
| A、CuCl2=Cu+Cl2↑ |
| B、H2SO4=2H++S6++4O2- |
| C、Na2CO3=2Na++CO32- |
| D、Ba(OH)2=Ba+2OH |
下列离子方程式与所述事实相符且正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- | ||||
B、用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-
| ||||
| C、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- | ||||
| D、稀硫酸滴在铜片上:Cu+2H+→Cu2++H2↑ |
下列物质中不属于混合物的是( )
| A、胶体 | B、淀粉 | C、王水 | D、水晶 |
下列判断正确的是( )
| A、原子形成具有相同电子层结构的离子后,原子序数小的离子半径一定大 |
| B、同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
| C、氯化氢的沸点比氟化氢的沸点高 |
| D、从HF、HCI、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增的规律 |