题目内容
19.已知O的电负性为3.5,Cl为3.1,但Cl2远比O2活泼,请加以解释.分析 分子的活泼性与分子中原子间形成的共价键的键能大小有关,键能越大,分子越稳定,据此分析.
解答 解:分子的活泼性与分子中原子间形成的共价键的键能大小有关,键能越大,分子越稳定,O2和Cl2分子参加反应前必须破坏共价键,即先拆成原子,因为O2中键能远大于Cl2,尽管O原子比Cl原子活泼,但O 2分子参加反应却比较困难.
答:O2和Cl2分子参加反应前必须破坏共价键,即先拆成原子,因为O2中键能远大于Cl2,尽管O原子比Cl原子活泼,但O 2分子参加反应却比较困难.
点评 本题考查了分子的稳定性与键能的关系,题目难度不大,侧重于基础知识的考查,注意把握化学变化的实质是旧键的断裂和新键的形成.

练习册系列答案
相关题目
19.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 62gNa2O溶于水后所得溶液中含有的O2-数为NA | |
| B. | 46gNO2和46gN2O4中含有的原子数均为3NA | |
| C. | 标准状况下,33.6L氟化氢中含有的氟原子数为1.5NA | |
| D. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2的分子数为0.46NA |
7.下列说法正确的是( )


| A. | 按系统命名法命名,图1化合物的名称是2,4,6一三甲基-5-乙基庚烷 | |
| B. | 图2有机物的一种芳香族同分异构体能发生银镜反应 | |
| C. | 图2有机物能使酸性高锰酸钾溶液褪色 | |
| D. | 图3为髙分子化合物,其单体为对苯二甲酸和乙二醇 |
4.一种烃的结构可表示为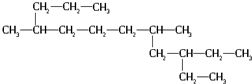 ,用系统命名法命名,该烃的名称为( )
,用系统命名法命名,该烃的名称为( )
 ,用系统命名法命名,该烃的名称为( )
,用系统命名法命名,该烃的名称为( )| A. | 4,8-二甲基-10-乙基12烷 | B. | 5,9-二甲基-3-乙基十二烷 | ||
| C. | 5-甲基-3-乙基-9-丙基十一烷 | D. | 3,9-二甲基-4-乙基十二烷 |
11.下列有关表述正确的是( )
| A. | 次氯酸的结构式H-Cl-O | |
| B. | 氯化钠的分子式:NaCl | |
| C. | F-的最外层电子排布式:2s22p5 | |
| D. | D216O中,质量数之和是质子数之和的两倍 |
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O中所含原子总数为NA | |
| B. | 质量均为7.8 g的Na2S、Na2O2固体中含有的阴离子数均为0.1NA | |
| C. | 标准状况下,2.24 L Cl2通入足量H2O,转移的电子数均为0.1NA | |
| D. | 常温下,浓度为0.01mol/L的Na2CO3溶液中CO32-的数目为0.01 NA |
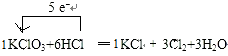 .
.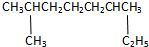 的系统命名是:2,6-二甲基辛烷
的系统命名是:2,6-二甲基辛烷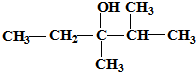 键线式是2,3-二甲基-3-戊醇
键线式是2,3-二甲基-3-戊醇 .
.