题目内容
2.下列说法不正确的是( )| A. | 除去96%的乙醇中的少量水制无水乙醇:加入生石灰,振荡、静置、蒸馏 | |
| B. | 除去溴苯中混有的少量单质溴:加入足量的NaOH溶液,振荡、静置、分液 | |
| C. | CH4和CCl4中的化学键均为非极性键,CH4、CCl4都是正四面体结构 | |
| D. | 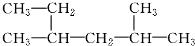 系统命名法为:2,4-二甲基-己烷 系统命名法为:2,4-二甲基-己烷 |
分析 A.CaO与水反应后,增大与乙醇的沸点差异;
B.溴与NaOH溶液反应后,与溴苯分层;
C.CH4和CCl4中的化学键分别为C-H极性键、C-Cl极性键,均为正四面体;
D.最长碳链含6个C,2、4号C上有甲基.
解答 解:A.CaO与水反应后,增大与乙醇的沸点差异,则加CaO、蒸馏可除去96%的乙醇中的少量水制无水乙醇,故A正确;
B.溴与NaOH溶液反应后,与溴苯分层,然后分液可除去溴苯中混有的少量单质溴,故B正确;
C.CH4和CCl4中的化学键分别为C-H极性键、C-Cl极性键,均为正四面体,不存在非极性键,故C错误;
D.最长碳链含6个C,2、4号C上有甲基,则名称为2,4-二甲基-己烷,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握物官能团与性质的关系、化学键、混合物分离方法为解答的关键,侧重分析与应用能力的考查,注意除杂及性质的应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列化学用语正确的是( )
| A. | H2S的电子式: | B. | Mg2+的结构示意图: | ||
| C. | Na2O的电子式: | D. | N2的电子式: |
1.下列说法中正确的是( )
| A. | 铁是黑色金属,所以断口是黑色的 | B. | 铁是第ⅧB族元素,也是过渡元素 | ||
| C. | 在自然界中无游离态的铁存在 | D. | 自然界里含铁的矿物质叫铁矿石 |
7.下列事实一定能说明HF是弱酸的是( )
①常温下NaF溶液的pH大于7
②用HF溶液做导电性实验,灯泡很暗
③常温下0.1mol/L的HF溶液的pH为2.3
④HF能与Na2CO3溶液反应,产生CO2气体
⑤HF与水能以任意比混溶
⑥1mol/L的HF水溶液能使紫色石蕊试液变红.
①常温下NaF溶液的pH大于7
②用HF溶液做导电性实验,灯泡很暗
③常温下0.1mol/L的HF溶液的pH为2.3
④HF能与Na2CO3溶液反应,产生CO2气体
⑤HF与水能以任意比混溶
⑥1mol/L的HF水溶液能使紫色石蕊试液变红.
| A. | ①③ | B. | ②③⑤ | C. | ④⑥ | D. | ①②⑤ |
14.元素周期表中某区域的一些元素多用于制造催化剂及耐高温材料,它们是( )
| A. | 稀有气体元素 | |
| B. | 过渡元素 | |
| C. | 氟、氯、硫、磷元素 | |
| D. | 金属元素和非金属元素分界线附近的元素 |
11.某溶液中有NH4+、Mg2+、Fe2+、Fe3+和NO3-五种离子,向该溶液的中加入过量的氢氧钠溶液,微热并搅拌,再加入过量盐酸,则溶液中大量减少的阳离子是( )
①Fe3+②Mg2+③Fe2+④NH4+.
①Fe3+②Mg2+③Fe2+④NH4+.
| A. | 只有①③ | B. | 只有①④ | C. | 只有②④ | D. | 只有③④ |
12.下列说法中错误的是( )
| A. | 氧元素位于第2周期VIA族 | |
| B. | 元素周期表中有7个主族、7个副族 | |
| C. | 稀有气体元素原子的最外层电子数均为8 | |
| D. | 铷、氯、锗三种元素中,适合作半导体材料的是锗 |
 校化学研究性学习小组查阅资料了解到以下内容:
校化学研究性学习小组查阅资料了解到以下内容: ,请配平该反应的离子方程式:
,请配平该反应的离子方程式: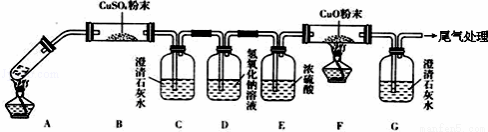
 若不能应怎样改进?______________.
若不能应怎样改进?______________.