题目内容
1.含氯消毒液(主要成分NaClO)与含氯洁厕灵(主要成分HCl)混用可能会造成中毒,其原因是:NaClO+2HCl═Cl2↑+NaCl+H2O.下列说法中正确的是( )| A. | NaCl是还原产物 | |
| B. | NaClO只含有离子键 | |
| C. | 当释放(标况下)2.24L Cl2时,一定有6.02×1022个氯分子扩散到室内 | |
| D. | 使用消毒液时滴加食醋可加快作用发挥,其原因用离子方程式表示为 ClO-+CH3COOH═HClO+CH3COO- |
分析 A.反应中氯元素黄金+1价和-1价变化为0价,氧化产物和还原产物为氯气;
B.NaClO含Cl-O键;
C.当释放(标况下)2.24L Cl2时,计算物质的量,氯气溶于水和水发生反应;
D.滴加食醋,发生强酸制取弱酸的反应生成HClO.
解答 解:A.NaClO+2HCl═Cl2↑+NaCl+H2O,反应中还原产物为氯气,故A错误;
B.NaClO含Cl-O共价键及离子键,故B错误;
C.当释放(标况下)2.24L Cl2时,气体物质的量=$\frac{2.24L}{22.4L/mol}$=0.1mol,氯气从水溶液中挥出,氯气和水反应,能溶于水,氯分子扩散到室内数目小于6.02×1022个,故C错误;
D.滴加食醋,发生强酸制取弱酸的反应生成HClO,发生的离子反应为ClO-+CH3COOH=HClO+CH3COO-,故D正确;
故选D.
点评 本题考查含氯化合物,为高频考点,把握物质的构成、化学键、离子反应为解答的关键,侧重分析与应用能力的考查,注意选项C为易错点,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
12.常温常压下,下列物质为液态的是( )
| A. | Fe2O3 | B. | NaOH | C. | CH3CH3 | D. | Br2 |
9.下列说法合理的是( )
| A. | 阿司匹林是常用的抗酸药 | |
| B. | 铵态氮肥常与碱性物质如草木灰等混合施用 | |
| C. | 生石灰主要成分是酸性化合物 | |
| D. | 从海水中可提取溴 |
16.下列物质中,属于电解质的有( )
| A. | CH3CH2OH | B. | 水 | C. | 油脂 | D. | 过氧化钠 |
6.下列各组溶液中H+ 浓度最大的是( )
| A. | 0.15 mol/L的盐酸 | B. | 0.10mol/L的硫酸 | ||
| C. | 0.15 mol/L的醋酸 | D. | 0.10mol/L的氢硫酸 |
4.下列说法正确的是( )
| A. | 二氧化硫能使高锰酸钾酸性溶液迅速褪色 | |
| B. | 可以用澄清石灰水鉴别二氧化硫和二氧化碳 | |
| C. | 硫粉在过量的纯氧中燃烧可以生成三氧化硫 | |
| D. | 少量二氧化硫通入浓的氯化钙溶液中能生成白色沉淀 |
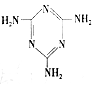 )俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸(
)俗称“蛋白精”.动物摄入三聚氰胺和三聚氰酸( 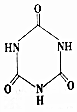 )
)