题目内容
在四只试剂瓶中分别盛放有KNO3溶液、K2CO3溶液、K2SO4溶液和KCl溶液,就如何检验这四种溶液分别回答下列问题.在四支试管中分别加入四种溶液各1ml,做下列实验.
(1)在四支试管里分别滴入稀硝酸,出现 现象的是 .
(2)在上述试验后剩余的三支试管中分别滴入 ,出现 现象的是 .
(3)在上述试验后剩余的两支试管中分别滴入 出现 现象的是 .
(1)在四支试管里分别滴入稀硝酸,出现
(2)在上述试验后剩余的三支试管中分别滴入
(3)在上述试验后剩余的两支试管中分别滴入
考点:物质的检验和鉴别的基本方法选择及应用
专题:
分析:KNO3溶液、K2CO3溶液、K2SO4溶液和KCl溶液,加盐酸检验碳酸钾会干扰KCl检验,则加硝酸检验碳酸钾,剩余三种物质中与硝酸钡反应生成沉淀的为K2SO4溶液,最后对剩余的两种物质中与硝酸银反应生成白色沉淀的为KCl,则另一无现象的为KNO3溶液,以此来解答.
解答:
解:(1)加盐酸检验碳酸钾会干扰KCl检验,则加稀硝酸检验碳酸钾,即出现气泡的为K2CO3溶液,发生的离子反应为CO32-+2H+=H2O+CO2↑,
故答案为:有气泡产生;K2CO3溶液;
(2)剩余三支试管中分别滴入Ba(NO3)2溶液,出现白色沉淀的是K2SO4溶液,发生的离子反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba(NO3)2溶液;白色沉淀;K2SO4溶液;
(3)剩余两支试管中分别滴入AgNO3溶液,出现白色沉淀的是KCl溶液,发生离子反应为Ag++Cl-=AgCl↓,而三次实验中都没有明显现象的是KNO3溶液,
故答案为:AgNO3溶液;白色沉淀;KCl溶液.
故答案为:有气泡产生;K2CO3溶液;
(2)剩余三支试管中分别滴入Ba(NO3)2溶液,出现白色沉淀的是K2SO4溶液,发生的离子反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba(NO3)2溶液;白色沉淀;K2SO4溶液;
(3)剩余两支试管中分别滴入AgNO3溶液,出现白色沉淀的是KCl溶液,发生离子反应为Ag++Cl-=AgCl↓,而三次实验中都没有明显现象的是KNO3溶液,
故答案为:AgNO3溶液;白色沉淀;KCl溶液.
点评:本题考查物质的鉴别和检验,为高频考点,把握物质的性质及检验时发生的反应、现象为解答的关键,注意检验物质中不能引入干扰离子,题目难度不大.

练习册系列答案
相关题目
工业用洗净的废铜作原料来制备硝酸铜.为了节约原料和防止污染,宜采取的方法是( )
A、Cu
| |||||
B、Cu
| |||||
C、Cu
| |||||
D、Cu
|
某组成为C5H12O的醇可被氧化成为C5H10O2的酸,具有这种结构的醇的同分异构体共有( )
| A、2种 | B、4种 | C、8种 | D、14种 |
短周期元素中,原子基态时具有1个未成对电子的元素共有多少种( )
| A、5 | B、6 | C、7 | D、8 |
某水溶液只可能含有K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-中的若干种离子.某同学取100m L的溶液分成两等份进行如下实验:
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲.
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体.
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到 11.65g固体.
下列结论正确的是( )
①第一份加过量的氢氧化钠溶液后加热,收集到0.02mol的气体,无沉淀产生,同时得到溶液甲.
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02g固体.
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到 11.65g固体.
下列结论正确的是( )
| A、实验①中产生的气体为氨气,并可得原溶液中c (NH4+)=0.2 mol?L-1 |
| B、实验③中的白色沉淀中一定有BaSO4,无BaCO3 |
| C、原溶液中一定有K+,且c (K+)=0.5 mol?L-1 |
| D、若要判断原溶液中是否有Cl-,无需另外设计实验验证 |
化学与生活、社会密切相关.下列说法错误的是( )
| A、亚硝酸盐属丁食物防腐剂,可以适量地添加于食物中 |
| B、氨气泄漏时,可喷洒大量的水以减少氨气的扩散 |
| C、漂白粉在空气中不稳定,可用于漂白纸张 |
| D、大量燃烧化石燃料是造成雾霾大气的重要原因 |
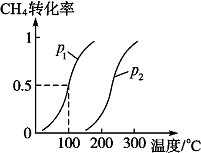 将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应Ⅱ:CH4(g)+H2O(g)?CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图.
将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),在一定条件下发生反应Ⅱ:CH4(g)+H2O(g)?CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图.