��Ŀ����
 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ��䵥�ʼ��������ڹ�ũҵ������������������Ҫ���ã�
���ǵ����Ϻ����ḻ��һ��Ԫ�أ��䵥�ʼ��������ڹ�ũҵ������������������Ҫ���ã���1��һ���¶��£���1L�ݻ��㶨���ܱ������г���2mol N2��8mol H2��������Ӧ��10min��ƽ�⣬��ð�����Ũ��Ϊ0.4mol/L����ʱ������ת����Ϊ
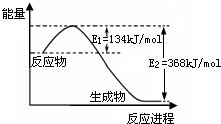
��2����ͼ��1mol NO2��g����1mol CO��g����Ӧ����1mol CO2��g����1mol NO��g�������������仯ʾ��ͼ����д���÷�Ӧ���Ȼ�ѧ����ʽ
��3��NH3��g��ȼ�յķ���ʽ4NH3��g��+7O2��g���T4NO2��g��+6H2O��l����
��֪��2H2��g��+O2��g���T2H2O��l����H=-483.6kJ/mol
N2��g��+2O2��g���T2NO2 ��g����H=+67.8kJ/mol
N2��g��+3H2��g���T2NH3 ��g����H=-92.0kJ/mol
�����NH3 ��g����ȼ����
��4��NO2����ˮ���գ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ
���÷�Ӧ6NO2+8NH3
| ���� |
| ���� |
��5����֪��2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ?mol-1
2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1
��ӦNO2��g��+SO2��g��?SO3��g��+NO��g���ġ�H=
һ�������£���NO2��SO2�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����
a����ϵѹǿ���ֲ���
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���
d��ÿ����1mol SO3��ͬʱ����1molNO2
���������Ӧƽ��ʱNO2��SO2�����Ϊ1��6����ƽ�ⳣ��K=
���㣺��ѧƽ��ļ���,�Ȼ�ѧ����ʽ,��ѧƽ��״̬���ж�
ר�⣺�����������������
��������1�����ݰ�����Ũ�ȼ��㵪����Ũ�ȱ仯����������ת����=
��100%��
��2�����������仯ͼ����Ӧ�ȵ�������Ӧ�Ļ�ܼ�ȥ�淴Ӧ�Ļ�ܣ�
��3�����ݸ�˹���ɹ���Ŀ���Ȼ�ѧ����ʽ���ݴ˼���ȼ���ȣ�ע�ⰱ����ϵ��Ϊ1�����ɵ�ˮΪҺ̬��
��4������������ˮ��Ӧ���������һ�����������ݻ��ϼ۵ı仯��Ϸ���ʽ���㣻
��5�����ø�˹���ɼ��㷴Ӧ�ȣ��õ�ƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ������Ҳ���䣬����ƽ��ʱ�����ʵ�Ũ�ȣ��ɼ���ƽ�ⳣ����
| ������ |
| ��ʼ�� |
��2�����������仯ͼ����Ӧ�ȵ�������Ӧ�Ļ�ܼ�ȥ�淴Ӧ�Ļ�ܣ�
��3�����ݸ�˹���ɹ���Ŀ���Ȼ�ѧ����ʽ���ݴ˼���ȼ���ȣ�ע�ⰱ����ϵ��Ϊ1�����ɵ�ˮΪҺ̬��
��4������������ˮ��Ӧ���������һ�����������ݻ��ϼ۵ı仯��Ϸ���ʽ���㣻
��5�����ø�˹���ɼ��㷴Ӧ�ȣ��õ�ƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��䣬�ɴ�������һЩ������Ҳ���䣬����ƽ��ʱ�����ʵ�Ũ�ȣ��ɼ���ƽ�ⳣ����
���
�⣺��1��10min��ƽ�⣬��ð�����Ũ��Ϊ0.4mol/L��������Ũ�ȱ仯��Ϊ0.4mol/L��
=0.2mol/L���ʵ�����ת����=
��100%=10%��
�ʴ�Ϊ��10%��
��2���÷�Ӧ���ʱ��H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol�������Ȼ�ѧ����ʽΪNO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ?mol-1��
�ʴ�Ϊ��NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ?mol-1��
��3��NH3��g��ȼ�յķ���ʽΪ4NH3��g��+7O2��g���T4NO2��g��+6H2O��l������֪��
��2H2��g��+O2��g���T2H2O��l����H=-483.6kJ/mol
��N2��g��+2O2��g���T2NO2��g����H=+67.8kJ/mol
��N2��g��+3H2��g���T2NH3��g����H=-92.0kJ/mol
���ݸ�˹���ɣ����2-���2+���3�ã�4NH3��g��+7O2��g���T4NO2��g��+6H2O��l����
��H=2��67.8kJ/mol-2����-92.0kJ/mol��+3����-483.6kJ/mol��=-1131.2kJ/mol��
�ʰ�����ȼ����Ϊ
=282.8kJ/mol��
�ʴ�Ϊ��282.8kJ/mol��
��4������������ˮ��Ӧ���������һ����������Ӧ�Ļ�ѧ����ʽΪ3NO2+H2O=2HNO3+NO����Ӧ6NO2+8NH3
7N2+12H2O�У�6NO2��NԪ�ػ��ϼ۽��ͣ���+4�۽��͵�0�ۣ���6molNO2�μӷ�Ӧ��ת��24mol���ӣ����Ե�ת��1.2mol����ʱ������NO20.3mol�����Ϊ6.72L���ʴ�Ϊ��6.72��
��5����֪����2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ?mol-1
��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1�����ø�˹���ɽ��١�
-�ڡ�
���õ��Ȼ�ѧ����ʽΪ��NO2��g��+SO2��g��?SO3��g��+NO��g��
��H=
����-196.6kJ?mol-1��-
����-113.0kJ?mol-1��=-41.8kJ?mol-1��
a�������Ƿ�ﵽƽ�⣬��ϵѹǿ�����ֲ��䣬���������ж��Ƿ�ﵽƽ��״̬����a����
b�����������ɫ���ֲ��䣬˵��Ũ�Ȳ��䣬�ﵽƽ��״̬����b��ȷ��
c��SO3��NO�ļ�����֮��Ϊ1��1�������Ƿ�ﵽƽ�⣬���ߵ�����ȱ��ֲ��䣬�����ж��Ƿ�ﵽƽ��״̬����c����
d�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ���ÿ����1mol SO3��ͬʱ����1molNO2�������ж��Ƿ�ﵽƽ��״̬����d����
��������b��ȷ��
NO2��g��+SO2��g��?SO3��g��+NO��g��
��ʼ���ʵ���� a 2a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� a-x 2a-x x x
ƽ��ʱNO2��SO2�����Ϊ1��6������1a-x������2a-x��=1��6����x=
a����ƽ�ⳣ��K=
=
=
=
��
�ʴ�Ϊ��-41.8��b��
��
| 1 |
| 2 |
| 0.2mol/L |
| 2mol/L |
�ʴ�Ϊ��10%��
��2���÷�Ӧ���ʱ��H=E1-E2=134KJ/mol-368KJ/mol=-234KJ/mol�������Ȼ�ѧ����ʽΪNO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ?mol-1��
�ʴ�Ϊ��NO2��g��+CO��g��=CO2��g��+NO��g����H=-234kJ?mol-1��
��3��NH3��g��ȼ�յķ���ʽΪ4NH3��g��+7O2��g���T4NO2��g��+6H2O��l������֪��
��2H2��g��+O2��g���T2H2O��l����H=-483.6kJ/mol
��N2��g��+2O2��g���T2NO2��g����H=+67.8kJ/mol
��N2��g��+3H2��g���T2NH3��g����H=-92.0kJ/mol
���ݸ�˹���ɣ����2-���2+���3�ã�4NH3��g��+7O2��g���T4NO2��g��+6H2O��l����
��H=2��67.8kJ/mol-2����-92.0kJ/mol��+3����-483.6kJ/mol��=-1131.2kJ/mol��
�ʰ�����ȼ����Ϊ
| 1131.2KJ/mol |
| 4 |
�ʴ�Ϊ��282.8kJ/mol��
��4������������ˮ��Ӧ���������һ����������Ӧ�Ļ�ѧ����ʽΪ3NO2+H2O=2HNO3+NO����Ӧ6NO2+8NH3
| ||
| �� |
��5����֪����2SO2��g��+O2��g��?2SO3��g����H=-196.6kJ?mol-1
��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1�����ø�˹���ɽ��١�
| 1 |
| 2 |
| 1 |
| 2 |
��H=
| 1 |
| 2 |
| 1 |
| 2 |
a�������Ƿ�ﵽƽ�⣬��ϵѹǿ�����ֲ��䣬���������ж��Ƿ�ﵽƽ��״̬����a����
b�����������ɫ���ֲ��䣬˵��Ũ�Ȳ��䣬�ﵽƽ��״̬����b��ȷ��
c��SO3��NO�ļ�����֮��Ϊ1��1�������Ƿ�ﵽƽ�⣬���ߵ�����ȱ��ֲ��䣬�����ж��Ƿ�ﵽƽ��״̬����c����
d�����ʵ���֮�ȵ��ڻ�ѧ������֮�ȣ���ÿ����1mol SO3��ͬʱ����1molNO2�������ж��Ƿ�ﵽƽ��״̬����d����
��������b��ȷ��
NO2��g��+SO2��g��?SO3��g��+NO��g��
��ʼ���ʵ���� a 2a 0 0
ת�����ʵ���� x x x x
ƽ�����ʵ���� a-x 2a-x x x
ƽ��ʱNO2��SO2�����Ϊ1��6������1a-x������2a-x��=1��6����x=
| 4 |
| 5 |
| c(SO3)c(NO) |
| c(NO2)c(SO2) |
| x2 |
| (a-x)(2a-x) |
(
| ||||
(a-
|
| 8 |
| 3 |
�ʴ�Ϊ��-41.8��b��
| 8 |
| 3 |
������������NO2��SO2��CO������Ϊ���壬�ۺϿ��黯ѧƽ���ƶ�����˹�����Լ�ƽ�ⳣ���ļ�������⣬������ѧ���ۺ����û�ѧ֪ʶ�������Ŀ��飬��Ŀ�Ѷ��еȣ�ȼ���ȵļ���Ϊ�״��㣬ѧ�������ݸ�˹���ɼ��㷴Ӧ�ȣ�����ȼ���ȸ���ķ������㣮

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
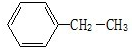
���и��������У�������ͬ���칹����ǣ�������
| A��CH3CH2OH��CH3-O-CH3 |
| B��H2NCH2COOH��CH3CH2NO2 |
| C��CH3CH2COOH��CH3COOCH3 |
| D��CH3CH3��CH3CH2CH3 |
��Ӧ2A��g��?2B��g��+C��g����H��0���ﵽƽ��ʱ��Ҫʹ����Ӧ��������A��Ũ������Ӧ��ȡ�Ĵ�ʩ�ǣ�������
| A����ѹ | B����ѹ |
| C������ | D��ʹ�ô��� |
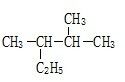
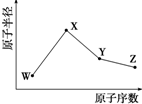 W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z��ԭ�Ӱ뾶��ͬ��������Ԫ������С��
W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����İ뵼����ϣ�Z��ԭ�Ӱ뾶��ͬ��������Ԫ������С��