题目内容
反应2A(g)?2B(g)+C(g)△H>0,达到平衡时,要使正反应速率增大,A的浓度增大,应采取的措施是( )
| A、减压 | B、加压 |
| C、升温 | D、使用催化剂 |
考点:化学反应速率的影响因素,化学平衡的影响因素
专题:化学平衡专题
分析:要使正反应速率增大,可增大反应物浓度、增大压强、升高温度、加入催化剂等,A的浓度增大,可加入A、增大压强或降温,使平衡向逆反应方向移动,以此解答.
解答:
解:A.减压,反应速率减小,故A错误;
B.加压,反应速率增大,平衡向逆反应方向移动,A的浓度增大,故B正确;
C.升高温度,反应速率增大,平衡向正反应方向移动,A的浓度减小,故C错误;
D.使用催化剂,平衡不移动,A的浓度不变,故D错误.
故选B.
B.加压,反应速率增大,平衡向逆反应方向移动,A的浓度增大,故B正确;
C.升高温度,反应速率增大,平衡向正反应方向移动,A的浓度减小,故C错误;
D.使用催化剂,平衡不移动,A的浓度不变,故D错误.
故选B.
点评:本题考查外界条件对化学平衡的影响,为高频考点,侧重于学生的分析能力能力的考查,难度不大,本题注意根据反应方程式的特征判断平衡移动的方向.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
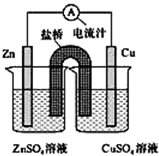 如图为一原电池的装置示意图,下列说法不正确的是( )
如图为一原电池的装置示意图,下列说法不正确的是( )| A、原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| B、原电池工作时,电流由铜极流经电流计流向锌极 |
| C、原电池工作时,盐桥中K+移向CuSO4溶液 |
| D、如果将Cu电极与Zn电极互换,电流计指针反向偏转 |
若阿伏伽德罗常数是NA,则下列说法不正确的是( )
| A、22g乙醛中含有σ键3NA |
| B、1.0L 0.1mol/L Na2S溶液中阴离子总数小于0.1NA |
| C、对于Si+O2=SiO2,每当形成2NA个Si-O键,需断开NA个Si-Si键 |
| D、某核素Cl的质量数为a,其摩尔质量为aNA g/mol |
下列各组离子,能在水溶液中大量共存的是( )
| A、OH-、K+、Fe3+、NO3- |
| B、HCO3-、OH-、Cl-、K+ |
| C、Mg2+、NO3-、H+、Al3+ |
| D、SO42-、Ag+、NH4+、Cl- |
氧化还原反应在生产、生活中具有广泛的用途.下列事例不属于氧化还原反应的是( )
| A、工业炼铁 | B、食醋除水垢 |
| C、食物消化 | D、木柴生火 |
下列关于摩尔的说法和使用正确的是( )
| A、物质的数量单位 |
| B、物质的量的单位 |
| C、1mol氧 |
| D、1mol大米 |
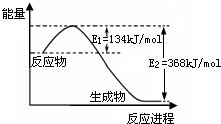 氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.