题目内容
现有mg某气体,它由双原子分子构成,它的摩尔质量为M g?mol-1.若阿伏加德罗常数用NA表示,则:
(1)该气体的物质的量为 mol,
(2)该气体所含原子总数为 个,
(3)该气体在标准状况下的体积为 L,
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为 ,
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为 ,
(6)在V L溶液中取出100mL,则含该气体溶质为 mol.
(1)该气体的物质的量为
(2)该气体所含原子总数为
(3)该气体在标准状况下的体积为
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为
(5)该气体溶于水后形成V L溶液,其溶液的物质的量浓度为
(6)在V L溶液中取出100mL,则含该气体溶质为
考点:物质的量的相关计算
专题:计算题
分析:结合n=
=
=
=cV计算相关物理量,以此解答.
| m |
| M |
| V |
| Vm |
| N |
| NA |
解答:
解:(1)m g某气体的物质的量为
=
mol,故答案为:
;
(2)因为一个分子中含两个原子,所以含有的原子数为分子数的2倍,即为2×
mol×NAmol-1=
,故答案为:
;
(3)该体积的体积为
mol×22.4L/mol=
L,故答案为:
;
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为ω=
×100%=
×100%,故答案为:
×100%;
(5)所得溶液的物质的量浓度=
=
mol/L,故答案为:
;
(6)在V L溶液中取出100mL,则含该气体溶质的物质的量为0.1L×
mol/L=
mol,故答案为:
.
| m g |
| M g/mol |
| m |
| M |
| m |
| M |
(2)因为一个分子中含两个原子,所以含有的原子数为分子数的2倍,即为2×
| m |
| M |
| 2mNA |
| M |
| 2mNA |
| M |
(3)该体积的体积为
| m |
| M |
| 22.4m |
| M |
| 22.4m |
| M |
(4)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为ω=
| mg |
| (1000+m)g |
| m |
| 1000+m |
| m |
| 1000+m |
(5)所得溶液的物质的量浓度=
| ||
| V L |
| m |
| MV |
| m |
| MV |
(6)在V L溶液中取出100mL,则含该气体溶质的物质的量为0.1L×
| m |
| MV |
| 0.1m |
| MV |
| 0.1m |
| MV |
点评:本题考查常用化学计量的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,题目比较基础,注意对公式的理解与灵活应用.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
下列各组金属均有导线相连,并插入对应的液体中,其中不能组成原电池的是( )
| A、Zn|H2SO4(稀)|Fe |
| B、Cu|AgNO3(aq)|Ag |
| C、Zn|CCl4|Cu |
| D、Fe|H2SO4(稀)|C |
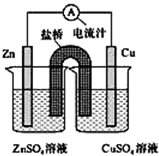 如图为一原电池的装置示意图,下列说法不正确的是( )
如图为一原电池的装置示意图,下列说法不正确的是( )| A、原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| B、原电池工作时,电流由铜极流经电流计流向锌极 |
| C、原电池工作时,盐桥中K+移向CuSO4溶液 |
| D、如果将Cu电极与Zn电极互换,电流计指针反向偏转 |
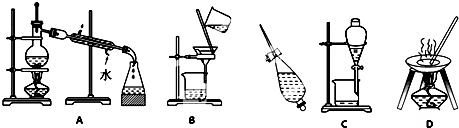
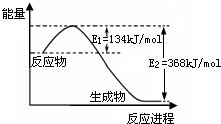 氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,其单质及化合物在工农业生产、生活中有着重要作用.