题目内容
17.有下列物质:①Fe ②Na2O ③CO2 ④Cu(OH)2 ⑤MgCl2⑥NH4Cl ⑦H2SO4 ⑧C2H5OH(酒精)⑨CO⑩蔗糖(用序号作答)(1)按组成分类,属于单质的是①;属于酸性氧化物的是③;属于碱性氧化物的是②;属于碱的是④;属于盐的是⑤⑥.属于酸的是⑦.
(2)上述十种物质中,其中属于电解质的有②④⑤⑥⑦,属于非电解质的有③⑧⑨⑩.
(3)写出上述物质中有硫酸参与的复分解反应的化学方程式Na2O+H2SO4=Na2SO4+H2O;Cu(OH)2+H2SO4=CuSO4+H2O.
分析 (1)(2)单质是有同种元素组成的纯净物;
酸性氧化物是和碱反应生成盐和水的氧化物;
碱性氧化物是和酸反应生成盐和水的氧化物;
酸是水溶液中电离出的阳离子全部是氢离子的化合物;
碱是水溶液中电离出的阴离子全部是氢氧根离子的化合物;
盐是金属阳离子和酸根阴离子构成的化合物,铵盐例外;
电解质指在水溶液中或熔融状态下能够导电的化合物;在上述两种情况下都不能导电的化合物称为非电解质;单质,混合物既不是电解质也不是非电解质;
(3)根据复分解反应的条件写出方程式.
解答 解:(1)(2)①Fe由一种元素组成的纯净物,属于单质,不是电解质;
②Na2O能和酸反应生成盐和水,属于碱性氧化物,属于电解质;
③CO2能和碱反应生成盐和水,属于酸性氧化物,CO2不能导电,不能电离出自由移动的离子,属于非电解质;
④Cu(OH)2电离出的阴离子全部是氢氧根离子,属于碱,属于电解质;
⑤MgCl2能电离出金属离子和酸根离子,是盐,属于电解质;
⑥NH4Cl是能电离出铵根离子和酸根离子,是盐,属于电解质;
⑦H2SO4电离出的阳离子全部是氢离子,是酸,属于电解质;
⑧C2H5OH(酒精)不能导电,不能电离出自由移动的离子,属于非电解质;
⑨CO不能导电,不能电离出自由移动的离子,属于非电解质;
⑩蔗糖不能导电,不能电离出自由移动的离子,属于非电解质;
故答案为:(1)①;③;②;④;⑤⑥;⑦
(2)②④⑤⑥⑦;③⑧⑨⑩;
(3)述物质中有硫酸参与的复分解反应有:Na2O+H2SO4=Na2SO4+H2O;Cu(OH)2+H2SO4=CuSO4+H2O;
故答案为:Na2O+H2SO4=Na2SO4+H2O;Cu(OH)2+H2SO4=CuSO4+H2O.
点评 本题考查了电解质与非电解质、导电性判断,题目难度不大,明确电解质与电解质的概念为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

| A. | 相同温度下,1 mol•L-1醋酸溶液与0.5 mol•L-1醋酸溶液中,c(H+)之比是2:1 | |
| B. | 向醋酸钠溶液中加入适量醋酸,使混合液的pH=7,此时混合液中c(Na+)=c(CH3COO-) | |
| C. | 保存FeSO4溶液时,应在其中加入稀HNO3以抑制Fe2+水解 | |
| D. | 0.1 mol•L-1NH4Cl溶液中c(NH4+)+c(H+)=c(Cl-) |
Ⅰ、(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成CaO•3MgO•4SiO2
(2)高分子材料可以分成无机高分子材料和有机高分子材料.
[Al Fe (OH)nCl6-n]m属于无机高分子材料,是一种新型高效净水剂,它广泛应用生活用水和工业污水的处理,其中铁元素的化合价为+3
Ⅱ、高纯二氧化硅可用来制造光纤.某稻壳灰的成分为:此空多余
| 组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
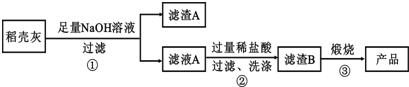
请回答下列问题:
(1)根据氧化物的性质进行分类,稻壳灰中涉及的氧化物最多有3类.
(2)步骤①中涉及SiO2的离子反应方程为SiO2+2OH-═SiO32-+H2O
(3)滤渣A的成分有C和Fe2O3(填化学式)
(4)步骤②洗涤沉淀的方法是:向漏斗中加水至浸没沉淀,待水自然流下后,再重复2-3次
(5)步骤③反应的化学方程式为:H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O;实验室进行步骤③用到的仪器有坩埚、泥三角、酒精灯、坩埚和泥三角.
| A. | ①②④ | B. | ②④⑤ | C. | ④⑤ | D. | ①② |
| 温度 | K |
| 973K | 1.47 |
| 1173K | 2.15 |
(2)该反应平衡常数的表达式为K=$\frac{C(CO)}{C(C{O}_{2})}$.
| 内容 | NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 |
| A | 发生水解 | 无银镜反应 | 不反应 | 不反应 |
| B | 发生中和反应 | 无银镜反应 | 溶解 | 放出H2 |
| C | 不反应 | 有银镜反应 | 有红色沉淀 | 放出H2 |
(1)此推出A、B、C的结构简式:A、CH3COOCH3、B、CH3CH2COOH、C、CH2(OH)CH2CHO
写出下列反应方程式
(2)A+NaOH:CH3COOCH3+NaOH→CH3COONa+CH3OH
(3)C+Cu(OH)2(新制):CH2(OH)CH2CHO+2Cu(OH)2$\stackrel{△}{→}$CH2(OH)CH2COOH+Cu2O↓+H2O
(4)C+Na:2CH2(OH)CH2CHO+2Na→2CH2(ONa)CH2CHO+H2↑.
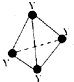 已知X的电负性在同主族元素中最大,其基态原子最外电子层的p轨道呈半充满状态.回答下列问题:
已知X的电负性在同主族元素中最大,其基态原子最外电子层的p轨道呈半充满状态.回答下列问题: