��Ŀ����
7��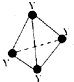 ��֪X�ĵ縺����ͬ����Ԫ����������̬ԭ��������Ӳ��p����ʰ����״̬���ش��������⣺
��֪X�ĵ縺����ͬ����Ԫ����������̬ԭ��������Ӳ��p����ʰ����״̬���ش��������⣺��1��XԪ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p3��X2�����ЦҼ���м��ĸ���֮��Ϊ1��2��
��2��X�������̬�⻯������У�Xԭ�ӵ��ӻ���ʽΪsp3�÷��ӵ����幹��Ϊ�����Σ�
��3����֪Si3X4����ԭ�Ӿ��壬�þ�����ܾ��е�������c������ţ���
a�����нϵ͵��۵� b���������õĵ����� c�����нϴ��Ӳ��
��4��YΪXͬ�����������ڵ�Ԫ�أ�����һ��ͬ��������ķ���ʽΪY4���ṹ��ͼ��ʾ���ڸ÷����У�����Y-Y��֮��ļ���Ϊ600�������һ��Y4���ӵ�ÿ��Y-Y���ж�����һ����ԭ�ӣ���һ���ɲ���6����ԭ�ӣ����û�����ķ���ʽΪP4O6��
���� ��֪X�ĵ縺����ͬ����Ԫ����������̬ԭ��������Ӳ��p����ʰ����״̬����p�����3�����ӣ�ӦΪNԪ�أ�
��1��XΪNԪ�أ�ԭ�Ӻ�����7�����ӣ���Ӧ�ĵ��ʽṹΪN��N��
��2��X�������̬�⻯�����ΪNH3�������к���3���Ҽ���1���µ��Ӷԣ�
��3��ԭ�Ӿ�����нϴ��Ӳ�ȣ������磻
��4��YΪXͬ�����������ڵ�Ԫ�أ�����һ��ͬ��������ķ���ʽΪY4��Ϊ���ף�Ϊ��������ṹ������Ϊ600���Դ˽����⣮
��� �⣺��֪X�ĵ縺����ͬ����Ԫ����������̬ԭ��������Ӳ��p����ʰ����״̬����p�����3�����ӣ�ӦΪNԪ�أ�
��1��XΪNԪ�أ�ԭ�Ӻ�����7�����ӣ���̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p3����Ӧ�ĵ��ʽṹΪN��N������1���Ҽ���2���м����Ҽ���м�������Ϊ1��2��
�ʴ�Ϊ��1s22s22p3��1��2��
��2��X�������̬�⻯�����ΪNH3�������к���3���Ҽ���1���µ��Ӷԣ�Ϊsp3�ӻ����÷��ӵ����幹��Ϊ�����Σ�
�ʴ�Ϊ��sp3�������Σ�
��3��ԭ�Ӿ�����нϴ��Ӳ�ȣ������磬�ʴ�Ϊ��c��
��4��YΪXͬ�����������ڵ�Ԫ�أ�����һ��ͬ��������ķ���ʽΪY4��Ϊ���ף�Ϊ��������ṹ������Ϊ600�������һ��Y4���ӵ�ÿ��Y-Y���ж�����һ����ԭ�ӣ���һ���ɲ��� 6����ԭ�ӣ����û�����ķ���ʽΪP4O6��
�ʴ�Ϊ��600��6��P4O6��
���� ���⿼��ṹ����λ�ù�ϵ�ۺ�Ӧ�ã��ƶ�Ԫ���ǽ���ؼ���ע���Ԫ�ػ�����֪ʶ���������գ�ע�����պ�������Ų����ɣ��ѶȲ���

| A�� | 0.5Q | B�� | Q | C�� | 2Q | D�� | 5Q |
| A�� | W g��ԭ���к���aNA��ԭ�� | |
| B�� | ����֪��Ϣ�ɵã�NA=$\frac{12}{a}$ | |
| C�� | ��ԭ�ӵ�Ħ��������aNA | |
| D�� | W g��ԭ�ӵ����ʵ���һ����$\frac{W}{a{N}_{A}}$mol |
| A�� | Ħ�������ʵ����ĵ�λ | B�� | Ħ�������������ĵ�λ | ||
| C�� | Ħ�������ĵ�λ�ǿ� | D�� | Ħ���������ʵ��� |
 ��
�� ��
��
